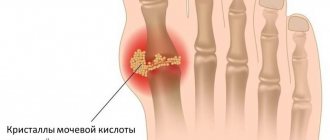
Подагра – это болезнь, связанная с нарушением обмена особых азотсодержащих веществ – пуриновых оснований. Пуриновые основания входят в состав нуклеиновых кислот – ДНК и РНК, отвечающих за хранение, передачу и реализацию наследственной информации в каждой клетке. При подагре в организм накапливается конечный продукт обмена пуриновых оснований – мочевая кислота.
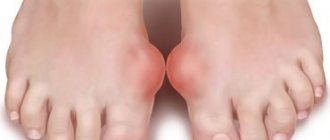
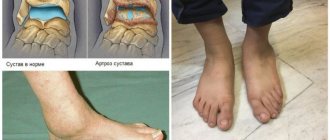
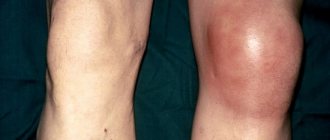
Мочевая кислота в избыточном количестве откладывается в виде кристаллов чаще всего с образование подагрических узлов (тофусов) в мелких суставах, вызывая их воспаление (подагрический артрит), а также в почках, что приводит к развитию мочекаменной болезни. На более поздних стадиях кристаллы мочевой кислоты откладываются и в других органах и тканях (особенно в хрящах, возле суставов).
Подагра сопровождается сильной болью в пораженных суставах (обычно это мелкие суставы пальцев стоп или рук), которая возникает под вечер, усиливается ночью и под утро затихает. При этом может наблюдаться повышение температуры – лихорадка.
Для лечения подагры используют особую группу лекарственных средств, которые называются противоподагрическими препаратами.
Классификация препаратов для лечения подагры
Противоподагрические препараты классифицируют на:
- средства, угнетающие образование мочевой кислоты (урикодепрессивные средства): аллопуринол, фебуксостат;
- средства, повышающие выведение мочевой кислоты (урикозурические средства): кислота лимонная + тринатрия цитрат + калия гидрокарбонат, сульфинпиразон, бензобромарон, пробенецид;
- противовоспалительные средства: колхицин, глюкокортикостероиды (преднизолон, триамцинолон, метилпреднизолон), нестероидные противовоспалительные средства (диклофенак, индометацин, напроксен, ибупрофен, кетопрофен, нимесулид).
Когда и кому Колхицин противопоказан. Совместимость с другими лекарствами
Несмотря на то, что это одно из лучших средств лечения подагры, у него есть ряд серьезнейших противопоказаний. Это также связано с тем, что действующее в-во колхицин относится к алколоидам и подобные «комбинации» могут вызвать серьезные нарушения в органах и тканях.
Лучшее средство от подагры – Колхицин
НИ В КОЕМ СЛУЧАЕ НЕЛЬЗЯ принимать его вместе с эритромицином, циклоспорином кларитромицином, а также блокаторами кальциевых каналов! Это может привести к самым печальным последствиям. Запрещено его сочетание с Дигоскином, статинами и фибратами. Категорически не рекомендуется пить и спиртное.
Противопоказано лечение с его помощью и при:
- повышенной чувствительности к алкалоидам;
- аллергической реакции на один из компонентов (и склонности к аллергии в целом);
- алкоголизме;
- хронических болезнях почек и печени;
- проблемах, связанных с костным мозгом;
- гнойных воспалениях.
Беременным и кормящим женщинам также нельзя пить эти таблетки. Пожилым людям и детям до 6 лет прием препарата назначают с особой осторожностью. К группе риска относятся и люди с серьезными проблемами жкт, а также те, кто страдает сердечно-сосудистыми заболеваниями. Препарат ухудшает усваивание организмом витамина В12.
Основы лечения подагры
Главную роль в лечении подагры играет диета. При подагре следует ограничить употребление в пищу продуктов, богатых пуринами – красное мясо, бобовые, сыр, творог, шоколад. Помимо этого, необходимо отказаться от приема алкоголя (особенно пива и вина).
При подагре важно поддерживать адекватный водный баланс – выпивать не мене двух литров воды в сутки. Особенно рекомендуется щелочное питье (чайная ложка соды на литр воды, щелочные минеральные воды), поскольку в щелочной среде мочи легче выводится мочевая кислота. В кислой же среде мочевая кислота выпадает в осадок в виде кристаллов и откладывается в почках.
Колхицин, глюкокортикостероиды и нестероидные противовоспалительные средства используют при остром приступе подагры.
В межприступный период, для снижения уровня мочевой кислоты в крови и профилактики приступов подагры применяют препараты, угнетающие образование мочевой кислоты – аллопуринол и фебуксостат.
Комбинированный препарат, содержащий кислоту лимонную, тринатрия цитрат и калия гидрокарбонат, назначают при мочекаменной болезни с целью подщелачивания мочи для облегчения растворения и выведения мочевых камней.
Таблетки от подагры, сэр
Вопреки шествующим один за другим экономическим кризисам, ухудшению экологической обстановки и снижению качества продуктов продолжительность жизни в большинстве стран мира растет. Мы стали жить дольше, а есть — вкуснее и разнообразней, чем каких-то полвека назад. Именно с этими тенденциями связывают рост распространенности подагры.
За последние 30 лет люди стали в 2 раза чаще страдать от болезни, причину которой определил еще до нашей эры знаменитый лекарь Гален, сказавший, что виной всему — несдержанность. Последователи Гаргантюа и Пантагрюэля, ценители вкусной, но не очень здоровой пищи обрекают себя на риск развития хронического артрита, для которого характерны периодически повторяющиеся крайне болезненные приступы воспаления, чаще всего — сустава у основания большого пальца.
Как по битому стеклу
Непосредственная причина воспалительного процесса при подагре — накопление в суставе острых, как осколки стекла, солей мочевой кислоты, уратов. Они физически повреждают суставную оболочку, что сопровождается мучительной болью, отеком и покраснением в зоне поражения.
Триггером, т. е. спусковым крючком, для развития приступа часто становится сытный обед или изобильный ужин. Именно с продуктами, в частности мясом, рыбой, кофе, чаем, алкоголем (особенно пивом), в организм поступают пурины, в результате разложения которых образуется мочевая кислота.
Подагра почти всегда приходит ночью, внезапно. Настигая любителя вкусной еды в постели, она нередко не позволяет ему покинуть спальню на протяжении нескольких дней — настолько сильна бывает боль. По окончании приступа, как правило, через 5–7 дней, уровень мочевой кислоты нормализуется, и подагра на какой-то период уходит сама собой.
К счастью, в наше время ждать неделю, изнывая от мучительной боли в тесных подагрических оковах, не нужно, ведь есть препараты, способные довольно быстро улучшить самочувствие.
И снова НПВП
Подагра — это артрит. А любое воспалительное заболевание суставов лечат прежде всего с помощью нестероидных противовоспалительных препаратов. Они не влияют на уровень мочевой кислоты, но позволяют достаточно быстро и эффективно купировать болевой синдром и снизить выраженность воспаления.
Группа НПВП обширна. И хотя все ее представители обладают как противовоспалительными, так и анальгетическими свойствами, при остром приступе подагры отдают предпочтение тем препаратам, который проявляют мощный и быстрый обезболивающий эффект: напроксену, кетопрофену, ибупрофену, диклофенаку и индометацину. Для достижения оптимального результата назначается максимальная дозировка препаратов на протяжении 10–14 дней, в зависимости от ответа на терапию.
При этом следует помнить, что на фоне приема НПВП могут развиваться желудочно-кишечные побочные эффекты, а потому людям, страдающим язвенной болезнью, гастритом и другими заболеваниями ЖКТ, средства этой группы могут быть противопоказаны.
Урикозурические препараты
Урикозурические препараты блокируют обратное всасывание мочевой кислоты в почечных канальцах, вследствие чего снижается ее уровень в крови. Но в то время как содержание уратов в суставах снижается, в моче их наоборот становится больше (они попросту фильтруются из крови в мочу). А это уже сопряжено с риском появления камней и развития почечнокаменной болезни.
К урикозурическим препаратам относятся колхицин и пробенецид. Они входят в международные рекомендации по лечению острого приступа подагры. Для того чтобы не допустить образования камней, колхицин и пробенецид назначают краткими курсами и в низких дозах. Впрочем, россиянам не придется переживать о переносимости урикозурических средств, поскольку на сегодняшний день они не зарегистрированы в нашей стране.
Блокаторы синтеза мочевой кислоты
Их название в фармакологии для большинства потребителей звучит весьма «тяжеловесно» — ингибиторы ксантиноксидазы. Впрочем, большинство страдающих подагрой знают это название наизусть и принимают соответствующие препараты.
К ингибиторам ксантиноксидазы относятся известный противоподагрический препарат аллопуринол, который сочетает довольно выраженную активность с доступностью, а также гораздо менее экономичный фебуксостат. И первый, и второй блокируют фермент, участвующий в синтезе мочевой кислоты, что приводит к снижению уровня уратов в крови.
Ингибиторы ксантиноксидазы назначают как для лечения, так и для профилактики приступов подагры (длительными курсами). Однако начало приема препаратов этой группы может спровоцировать обострение заболевания, поэтому их не рекомендуют назначать во время острого воспалительного процесса.
Ударить гормонами!
А вот препараты гормонов надпочечников, глюкокортикостероиды, в отличие от ингибиторов ксантиоксидазы как раз способны в краткие сроки и очень эффективно купировать острый приступ подагры. Однако назначают их далеко не всем и не всегда — слишком велик перечень побочных эффектов при системном приеме препаратов этой группы. Среди самых распространенных — отеки, выведение калия, кальция, повышение артериального давления, увеличение уровня глюкозы в крови, повышение свертываемости крови, нарушение менструального цикла.
Во избежание развития неблагоприятных реакций кортикостероидные гормоны назначают только тем, кто не переносит НПВП и колхицин, и только краткими курсами. Чаще всего с этой целью используют преднизолон, триамцинолон, кортикотропин в виде таблеток или инъекций.
Марина Поздеева
Фото depositphotos.com
Товары по теме: (напроксен), (кетопрофен), (ибупрофен), [product strict=»диклофенак»](диклофенак), [product strict=»аллопуринол»](аллопуринол), (фебуксостат), [product strict=»преднизолон»](преднизолон), (триамцинолон)
Лечение подагры: проблемы, парадоксы, перспективы
Журнал «Медицинский совет» №2/2020
DOI:
10.21518/2079-701X-2020-2-104-108
Интервью с ведущим экспертом в лечении подагры заведующим лабораторией микрокристаллических артритов ФГБНУ «Научно-исследовательский институт ревматологии имени В.А. Насоновой» кандидатом медицинских наук Максимом Сергеевичем Елисеевым.
Gout treatment: problems, paradoxes, prospects
Interview with a leading expert in the treatment of gout, head of the laboratory of microcrystalline arthritis of the Federal State Budget Scientific Institution “Scientific Research Institute of Rheumatology named after V.A. Nasonova“ candidate of medical sciences Maxim Sergeevich Eliseev.
- Максим Сергеевич, что можно сказать о значимости проблемы подагры в настоящее время? Каковы тенденции заболеваемости в России и в мире?
– Под подагрой в настоящее время понимают заболевание, которое проявляется острыми приступами артрита вследствие отложения кристаллов моноурата натрия в суставах на фоне повышенного уровня мочевой кислоты. Однако следует помнить, что кристаллы могут не только откладываться в суставах, но и поражать различные органы и системы, включая, например, сосуды. Поэтому проблема заключается не в том, чтобы просто вылечить острый артрит, а в том, чтобы справиться с системными проявлениями болезни, так как пациенты с подагрой значительно чаще умирают от сердечно-сосудистых заболеваний (ССЗ), страдают от болезней почек. В последние годы был проведен ряд исследований, которые ярко высветили эту проблему. Так, если 20 лет назад пациентов, госпитализируемых с подагрой, было намного меньше, чем больных с ревматоидным артритом (РА), то в настоящее время наблюдается обратная картина. В США, к примеру, пациентов с подагрой сегодня госпитализируется в 2 раза больше, чем с РА. Несмотря на то, что разрабатываются и активно внедряются новые лекарственные средства для лечения подагры, добиться явного прорыва пока не удалось. Если в терапии РА введение новых препаратов позволило достичь существенного прогресса, то в отношении подагры результата пока нет – мы топчемся на месте, в то время как затраты на лечение этих пациентов постоянно растут.
Что касается смертности, то ее показатели, опять же, при РА существенно снизились и постепенно приближаются к популяционным, тогда как при подагре такого не происходит. Главные причины – плохой контроль уровня мочевой кислоты (один из главных факторов риска заболевания почек и ССЗ) и сопутствующих заболеваний, таких как артериальная гипертензия, сахарный диабет (СД), нарушения липидного обмена. Основная часть пациентов, которых мы госпитализируем, – лица моложе 50 лет, и у большинства из них уже есть хронические тяжелые заболевания, которые и определяют будущий неблагоприятный исход.
Если говорить об уровне заболеваемости, то в развитых странах с высоким уровнем жизни частота подагры среди взрослого населения колеблется от 1 до 6%. В мужской популяции этот процент еще выше. В Великобритании, например, это 2,5%, в США – 4%, на Тайване – 6%. В РФ популяционные исследования распространенности подагры не проводились, но мы можем экстраполировать данные о распространенности гиперурикемии, учитывая, что в среднем каждый пятый пациент с гиперурикемией заболевает подагрой. Так вот, Россия по уровню распространенности гиперурикемии находится примерно посередине между Великобританией (13–14%) и США (20–21%), этот показатель у нас составляет около 17%. Если разделить его на 5, то получается, что примерно 3% взрослого населения в нашей стране страдает подагрой. В большинстве стран, где ведутся проспективные популяционные исследования, этот показатель либо продолжает расти, либо сохраняется на том же уровне. Если же рассматривать абсолютное число людей, страдающих болезнью, то суммарно оно увеличивается.
- Что, на Ваш взгляд, является причиной недостаточного контроля уровня мочевой кислоты?
– Я бы назвал одной из главных причин недостаточные знания врачей относительно того, как лечить пациента, чтобы добиться эффективного снижения уровня мочевой кислоты. Второй момент – это низкая приверженность к лечению самих пациентов, которые не всегда соблюдают предписания врача, даже если лечение назначено правильно. Еще одна причина – очень плохой контроль сопутствующих заболеваний. Например, при болезни почек лечение должно назначаться как можно раньше, и оно имеет определенные особенности. Есть некий парадокс. Добиться так называемой цели лечения (таргетный принцип терапии) при РА бывает очень трудно, для этого могут потребоваться колоссальные средства и длительный прием дорогостоящих препаратов, но сегодня ревматологи с этим успешно справляются. А при подагре добиться полного контроля над заболеванием можно в 90–95% случаев, но этого не происходит. И у врачей, и у пациентов есть мнение, ничем не подкрепленное, что подагра – болезнь неизлечимая. Даже специалисты не верят, что можно достичь прогресса и полностью изменить течение болезни. Хотя при подагре существует возможность абсолютного регресса даже костных эрозий и восстановления структуры костей при наличии внутрикостных тофусов: отложения кристаллов уратов и там могут полностью рассосаться. И, тем не менее, картина пока не меняется в лучшую сторону.
Представим ситуацию: пациент приходит к врачу, у него измерили уровень мочевой кислоты, назначили уратснижающий препарат, но не исследовали уровень холестерина, который повышен более чем у 50% больных с подагрой, а также уровень триглицеридов (он превышает норму более чем у 60% пациентов). СД среди больных подагрой встречается в несколько раз чаще, чем в популяции. В некоторых странах его частота достигает 20%, т.е. каждый пятый пациент с подагрой страдает еще и СД. Более ранняя диагностика этих состояний и соответствующее лечение могли бы улучшить прогноз заболевания, но этого почему-то не происходит. Проблему представляет и выбор оптимального лекарственного препарата, который может как позитивно, так и негативно влиять на уровень мочевой кислоты, а также знание совместимости большого количества разных медикаментов, назначаемых в связи с сопутствующими заболеваниями, в числе которых и ИБС, и сердечная недостаточность. И нужно быть очень грамотным специалистом, чтобы выбрать оптимальную стратегию лечения.
- Является ли подагра хорошо изученным заболеванием или остались какие-то белые пятна в понимании ее этиологии и патогенеза?
– Это заболевание хорошо изучено, и это второй парадокс. Первые упоминания о подагре встречаются в египетском папирусе Эберса, которому около 5 тысяч лет. То есть подагра описана как болезнь еще до Гиппократа. Были изложены основные принципы ее лечения, включая лечение колхицином, использование специальных эликсиров, которые могли уменьшить боль в суставах у больных. Подагрой страдало огромное количество известнейших людей, упоминание о ней есть у Гиппократа, Сиденгама – величайшего английского врача XVII века. Известнейший нидерландский ученый, изобретатель светового микроскопа и основоположник микроскопии Левенгук впервые обнаружил и описал кристаллы мочевой кислоты еще в XVII веке. Пожалуй, это самое древнее известное нам заболевание суставов. Но, тем не менее, белых пятен остается немало. До сих пор непонятно, почему подагрой заболевает только каждый пятый пациент с высоким уровнем мочевой кислоты. Причем линейной зависимости между уровнем мочевой кислоты и заболеваемостью тоже не наблюдается. Вполне возможно, и это сейчас изучается, существуют генетические факторы, которые в большей степени предрасполагают к развитию гиперурикемии, а есть те, которые отождествляются с большей вероятностью развития подагры, с кристаллизацией солей мочевой кислоты, без чего болезнь невозможна. Не совсем понятно, каким образом осуществляется самокупирование приступа. Иными словами, подагрическое воспаление развивается в рамках аутовоспалительного процесса, т.е. процесса, связанного с активацией кристаллами уратов определенных Toll-like рецепторов и, в конечном счете, синтеза белков, которые приводят к развитию иммунного процесса. Он характеризуется развитием острого нейтрофильного воспаления, однако не ясны механизмы, которые приводят к самокупированию этого воспаления.
До сих пор окончательно не выяснена роль мочевой кислоты. Ряд исследований демонстрирует, что она имеет безусловное значение в развитии ССЗ, заболеваний почек, но самостоятельно или в связи с отложением кристаллов – тоже не совсем ясно. В последних работах было показано, что у пациентов с повышенным уровнем мочевой кислоты, но без острого артрита кристаллы просто надо хорошо поискать, и в большинстве случаев они будут выявлены. А наличие кристаллов говорит о реализации иммунного ответа и, как следствие, развитии воспаления. Мочевая кислота в пробирке в больших концентрациях проявляет выраженные прооксидантные свойства и, следовательно, может способствовать развитию заболеваний сердечно-сосудистой системы и патологии почек. Насколько эти негативные эффекты могут быть реализованы в условиях организма, окончательно не ясно.
- Какие факторы риска заболевания можно выделить?
– Их можно разделить на две основные группы – немодифицируемые и модифицируемые. Первая группа – это генетические факторы, прежде всего те, что связаны с наличием нескольких уратных транспортеров, которые обеспечивают процесс реабсорбции мочевой кислоты в почках: URАТ-1, SLC-2А9, GLUT-9, ОАТ-4 и другие. И в меньшей степени те, которые связаны с экскрецией мочевой кислоты (ABCG2). Иными словами, 90% пациентов с подагрой – это люди, у которых не выводится мочевая кислота в силу генетической предрасположенности. Примерно 75% мочевой кислоты синтезируется в самом организме, а 20–25% поступает извне. На уровень мочевой кислоты оказывают влияние особенности питания, образ жизни и ряд заболеваний, а также прием лекарственных препаратов (мочегонные средства, некоторые препараты для лечения туберкулеза). К модифицируемым факторам риска также следует отнести прием алкоголя. Среди заболеваний, которые могут приводить к повышению уровня мочевой кислоты, – гипертоническая болезнь, сердечная недостаточность, почечная недостаточность, псориаз, миелопролиферативные заболевания. Следует отметить, что мужчины чаще страдают подагрой, чем женщины, по крайней мере до наступления менопаузы. Это объясняется тем, что эстрогены обладают способностью увеличивать экскрецию мочевой кислоты.
- Расскажите, пожалуйста, как развивается и протекает заболевание.
– Ряд ученых предложили последовательную, или ступенчатую, схему развития подагры. Первая стадия – асимптоматическая гиперурикемия. Для нее характерно повышение уровня мочевой кислоты, отсутствие кристаллов и поражения суставов. Можно назвать эту стадию предподагрой. Следующая стадия – отложение кристаллов мочевой кислоты на фоне гиперурикемии. Как это можно выявить? Например, при проведении пациенту рутинно УЗИ или компьютерной томографии (КТ) в связи с другой патологией. С помощью этих методов можно обнаружить кристаллы у 20–25% пациентов, особенно в нижних конечностях. Следующая стадия – гиперурикемия с отложением кристаллов и наличие острых приступов артрита, то есть собственно подагра. Болезнь продолжает прогрессировать, приступы повторяются, и заканчивается это тяжелым хроническим артритом с развитием подагрической артропатии, деформацией и ограничением функции суставов, а также поражением внутренних органов, связанным с отложением кристаллов мочевой кислоты. Остается не вполне понятным, насколько наличие кристаллов у пациентов с повышенным уровнем мочевой кислоты увеличивает риск развития подагры, приведет ли оно неизбежно к развитию болезни и когда это случится? С другой стороны, если исходно нет кристаллов, но есть гиперурикемия, какова вероятность того, что подагра не разовьется? Эти исследования только начинают проводить, и в ближайшее время мы вряд ли получим ответы на эти вопросы.
- Какие органы страдают при подагре?
– Помимо суставов, основными органами-мишенями являются сердечно-сосудистая система и почки. Практически в 100% случаев при подагре в них обнаруживают отложения кристаллов мочевой кислоты. Это не приводит к таким тяжелым проявлениям, как отложение кристаллов в суставе (острым приступам артрита, характеризующимся сильнейшей болью), но возникающее в сосудистой стенке, в почках воспаление развивается по тем же законам. И это, вероятно, главная причина, по которой пациенты с подагрой погибают от различных сердечно-сосудистых катастроф значительно чаще, чем пациенты без подагры. Гипотетически кристаллы мочевой кислоты можно найти в разных органах и системах. Так, у 40% пациентов с подагрой кристаллы обнаруживают в простате при оперативном вмешательстве, по данным гистологического исследования. Важно отметить, что в настоящее время подагра рассматривается как один из факторов риска развития рака предстательной железы.
- В чем особенности поражения почек при подагре?
– Традиционно считается, что при подагре обязательно происходит образование камней в почках. Однако исследования показали, что в целом камни в почках у пациентов с подагрой встречаются не чаще, чем в популяции. В основном это уратные камни, фосфатные же, струвитные, наоборот, встречаются реже. С другой стороны, те кристаллы, которые откладываются в почках, но не приводят к образованию камней, могут вызывать воспаление в канальцевом аппарате. На экскрецию мочевой кислоты влияют уратные транспортеры, количество которых генетически детерминировано. В норме 90% мочевой кислоты реабсорбируется в почках, а 10% выводится. Генетическая поломка приводит к тому, что этот процент снижается до 5–7. Отложение кристаллов мочевой кислоты может вызывать тубулоинтерстициальное воспаление по тому же механизму, что и в суставах. В конечном счете это воспаление может приводить к гибели нефронов, клеток почечных канальцев, развитию фиброзных изменений, а также, возможно, способствовать развитию амилоидоза.
Мочевая кислота может оказывать негативное влияние на ренин-ангиотензивную систему. Первые исследования, еще на крысах, показали, что при повышении уровня мочевой кислоты почки страдают в первую очередь. Страдают почки – повышается давление. Пробовали назначать препараты для снижения давления – ничего не происходило. Назначение уратснижающих препаратов приводило к нормализации давления и работы почек. В дальнейшем такой подход стали использовать в лечении подагры у людей. Практически во всех работах назначение препаратов, снижающих уровень мочевой кислоты, приводило к статистически достоверному снижению артериального давления (АД). И кристаллы, и сама мочевая кислота в канальцевом аппарате почек могут вызывать развитие воспаления и менять структуру почечных клеток, фенотипически они становятся другими. Это приводит к снижению функции и прогрессированию хронической болезни почек (ХБП).
До того, как научились лечить подагру, то есть до появления действенных уратснижающих препаратов, значительная часть пациентов (до 20–30%) погибала от острой уратной нефропатии. Сегодня такие ситуации встречаются гораздо реже. Когда уровень мочевой кислоты становится чрезвычайно высоким, что часто случается при миелопролиферативных заболеваниях, при назначении цитостатиков, происходит накопление огромного количества мочевой кислоты, которая просто «забивает» почечные канальцы. Единственное, что можно сделать – провести гемодиализ, раньше же использовали щелочные растворы (бикарбонат натрия). Другая ситуация – это хроническая нефропатия, когда вследствие формирования кристаллов возникает хроническое воспаление. И здесь сложно определить, от чего в большей степени страдают почки: от повышенного давления, высокого уровня глюкозы или же мочевой кислоты.
- Какой прогноз при подагрической нефропатии?
– Если болезнь не лечить, то у 45–50% пациентов с подагрой развивается клинически значимая хроническая болезнь почек. 10–15% лиц, страдающих подагрой, – пациенты с ХБП 3-й и более стадии, т.е. это кандидаты на проведение экстракорпорального лечения, заместительной терапии. Это намного выше, чем в популяции, и связано с неадекватным лечением болезни.
- Встречаются ли «сложные случаи» при диагностике подагрической нефропатии?
– Рутинно отделить хроническую болезнь почек, связанную с гипертонией или СД, от подагрической нефропатии, наверное, непросто. Предпринимаются попытки проводить исследования с привлечением новых инструментальных возможностей, сцинтиграфии, определения различных маркеров, но, к сожалению, они не специфичны для подагры. Речь идет, скорее, о том, чтобы заподозрить еще на предклинической стадии возможность развития проблемы как таковой, когда на нее можно повлиять. Если мы видим высокий уровень мочевой кислоты и, пусть минимально, снижение скорости клубочковой фильтрации (СКФ), целесообразно рассмотреть необходимость назначения адекватного лечения этих пациентов независимо от частоты приступов артрита и наличия/ отсутствия уратного нефролитиаза. На что обычно обращает внимание врач? На показатели крови, уровень креатинина, с помощью которого можно рассчитать скорость клубочковой фильтрации – это более объективный показатель, отражающий работу почек. На функцию почек может влиять прием лекарственных препаратов, наличие сопутствующих заболеваний и еще множество факторов. Так, например, подъем уровня мочевой кислоты способствует увеличению выработки ренина, в результате чего повышается давление, а это, в свою очередь, приводит к ухудшению работы почек и нарушению выведения мочевой кислоты. Образуется замкнутый круг. Что является первичным, а что вторичным в этой цепочке, сказать трудно.
- Если говорить о современных стандартах лечения подагрической нефропатии, каковы основные направления и цели терапии? Что является критерием эффективности противоподагрической терапии?
– Следует помнить, что в норме у человека каждый год погибает определенное количество нефронов, почки не восстанавливаются после повреждения так же активно, как печень. Попытка воздействовать на ключевые факторы риска является определяющей в профилактике подагрической нефропатии. Другими словами, если у пациента контролируются показатели АД, уровня гликемии, то нефропатия не будет прогрессировать. Устранив эти факторы риска, мы можем добиться как минимум стабилизации состояния и, возможно, улучшения работы почек на какое-то время. Поэтому исследования последних 20 лет направлены на коррекцию гиперурикемии как фактора риска развития и прогрессирования хронической почечной недостаточности (ХПН). Первые работы появились 1,5–2 десятилетия назад и отличались тем, что были проведены на ограниченном количестве пациентов и охватывали небольшой период времени. Но даже 6–12 месяцев было достаточно, чтобы говорить об относительно успешном применении препаратов, снижающих уровень мочевой кислоты. Последующие исследования, прежде всего применения аллопуринола, показали, что не все так очевидно. Во-первых, назначение аллопуринола не всегда приводило к замедлению прогрессирования ХБП по сравнению с контрольными группами. Использование высоких доз препарата лимитировалось риском развития нежелательных явлений у пациентов. Мы знаем, что аллопуринол в значительной степени экскретируется почками, как и один из его метаболитов оксипуринол. Это может увеличивать вероятность развития нежелательных явлений. Тем не менее эти работы продемонстрировали, что если мочевая кислота не снижается до целевого уровня, при котором образование кристаллов невозможно, глобально мало что изменится. Сам факт приема лекарственного препарата ничего не гарантирует. Как и в случае лечения других обменных заболеваний, мы должны опираться на конкретные цифры. Например, при сахарном диабете (СД) целью является достижение определенного уровня гликированного гемоглобина, у пациентов с гипертензией – целевое снижение показателей АД. Так и при подагре целью является снижение уровня мочевой кислоты до определенных значений, достижение которых и предопределит эффективность уратоснижающей терапии.
Если говорить об аллопуриноле, то препарат эффективен лишь на ранних стадиях, когда болезнь только начинается. Известно, что у половины пациентов с подагрой клинически значимо снижена скорость клубочковой фильтрации. У пациентов с запущенной стадией болезни эффект аллопуринола недостаточен. На низких дозах цель не удается достичь, а высокие дозы назначать нельзя из-за риска лекарственных осложнений. В последние 10 лет мы стали получать все больше информации о возможности применения фебуксостата, который в большей степени и быстрее способен снижать уровень мочевой кислоты, положительно влияя на СКФ, причем независимо от стадии ХБП. Эти исследования были продолжительными, что позволяет учитывать отдаленные исходы. В течение первых двух лет приема фебуксостата среднее значение СКФ может даже увеличиваться, чего не происходит при назначении аллопуринола. Максимальный период наблюдения на данный момент составляет 5 лет, и результаты показывают, что снижение функции почек у больных на фоне приема фебуксостата вполне сопоставимо с таковым у здорового человека с нормальными показателями мочевой кислоты. Причем это происходит как у пациентов с подагрой, так и с асимптоматической гиперурикемией.
- За счет чего достигается такой результат?
– За счет снижения уровня мочевой кислоты и ингибирования ксантиноксидазы, фермента, который участвует в этом процессе. Подавление этого фермента оказывает влияние на оксидантный стресс, уменьшая выработку активных молекул кислорода и увеличивая продукцию оксида азота. Это механизм защиты клетки и одновременно – снижение риска кардиоваскулярных катастроф у пациентов с ХБП, поскольку ХПН является одним из факторов риска общей кардиоваскулярной смертности пациентов с подагрой, а не только причиной развития терминальной почечной недостаточности. Если мы снижаем скорость прогрессирования ХБП, уменьшаются и кардиоваскулярные риски, пациент живет дольше.
Были проведены исследования, где сравнивали непосредственно аллопуринол и фебуксостат. Независимо от того, насколько выраженным было поражение почек, фебуксостат продемонстрировал определенные преимущества и у пациентов с терминальной стадией, и у пациентов с умеренным или выраженным снижением скорости клубочковой фильтрации, т.е. с 3, 4, 5-й стадией заболевания. По сути, лечение сейчас проводится в режиме монотерапии. Фебуксостат может быть эффективен даже в виде дополнения к гемодиализу. Оставшиеся нефроны работают дольше, и функция почек остается максимально сохранной. При СКФ ниже 30, когда считается, что уратснижающая терапия уже не работает, назначение фебуксостата даже в низких дозах (до 40 мг/сут) позволяет добиться хорошего результата. При этом препарат обладает очень хорошей переносимостью.
- Что, кроме медикаментозной терапии, сегодня используют в терапии подагрической почки?
– Обязательным является соблюдение низкосолевой диеты. Необходимо уменьшить потребление натрия и калия, белка. Но это, скорее, профилактика, которая существенно не влияет на прогноз. Предпринимаются попытки воздействия на факторы риска, которые до последнего времени были недостаточно изучены. Если мы снизим уровень мочевой кислоты, то сможем либо предотвратить, либо, в худшем случае, замедлить снижение СКФ. К профилактике следует отнести полный отказ от курения, алкоголя, назначение мочегонных препаратов.
- Какие возможности Вы видите для улучшения контроля заболевания?
– Если врачи будут строго следовать рекомендациям Ассоциации ревматологов России и Европейской антиревматической лиги по лечению подагры, а пациенты принимать назначенное им лечение, то, по нашим данным, которые в ближайшее время будут опубликованы, вероятность достижения целевых показателей мочевой кислоты может составлять 95%. При адекватном назначении ингибиторов ксантиноксидазы, фебуксостата проблема может быть решена. В оставшихся 5% случаев потенциально могут помочь препараты другого механизма действия, например урикозурики, препараты пегуриказы. Еще один ингибитор ксантиноксидазы – топироксостат разработан и используется в Японии. Существуют сахароснижающие препараты, которые понижают уровень мочевой кислоты, ингибиторы натрий-глюкозного котранспортера 2-го типа, тиазолидиндионы, некоторые липидснижающие (фенофибрат, розувастатин, аторвастатин) и гипотензивные препараты (лосартан), хотя их уратснижающий эффект весьма умеренный. Прошел третью стадию клинических исследований архалофенат – он снижает как уровень сахара, так и мочевой кислоты, а кроме того, обладает противовоспалительным действием.
Многие пациенты отказываются принимать уратснижающие препараты из-за большого числа назначенных им лекарств. При дозе 500 мг/сут нужно принимать до 5 таблеток аллопуринола в день, при этом необходимо титровать дозу, постепенно увеличивая количество таблеток в зависимости от уровня мочевой кислоты. В случае фебуксостата достаточно принимать 1 таблетку 80 мг, при этом в 2/3 случаев отсутствует необходимость увеличивать дозу.
Уратснижающая терапия не только может предотвратить развитие острых приступов артрита, но и снизить вероятность развития сердечно-сосудистых заболеваний. Если уровень мочевой кислоты ниже 360 мкмоль/л, смертность пациентов в 2 раза меньше в целом, а по причине кардиоваскулярных катастроф – в 2,5 раза. Это доказано результатами трехлетнего наблюдения более 1000 пациентов с подагрой, в ходе которого анализировалось влияние терапии на риск общей и сердечно-сосудистой смертности, опубликованного в 2019 году.
Помимо контроля уровня мочевой кислоты, важна и адекватная противовоспалительная терапия. Назначение того же колхицина у пациентов с высоким сердечнососудистым риском, по последним данным, снижает вероятность развития инфарктов, инсультов и тромбозов. То есть колхицин оказывает двойное действие – блокирует развитие воспаления как в суставах, так и в стенках сосудов.
В американском исследовании изучали ингибиторы интерлейкина-1, которые при длительном наблюдении продемонстрировали уменьшение риска сердечно-сосудистых катастроф на 15% у пациентов как с подагрой, так и с гиперурикемией. К сожалению, препарат не был зарегистрирован FDA, в первую очередь из-за высокой стоимости, а во-вторых, из-за того, что частота инфекционных осложнений была в целом выше, чем в популяции, что делает его использование нерациональным.
В заключение хотелось бы еще раз подчеркнуть, что адекватное применение уратснижающих препаратов, в первую очередь ингибиторов ксантиноксидазы, у пациентов с подагрой и асимптоматической гиперурикемией при наличии ХБП может реально замедлить прогрессирование ХБП и должно рассматриваться в качестве основного направления лечения.
Беседовала Людмила Головина
Метаболический синдром и подагра – подходы к антигипертензивной терапии
О статье
2953
0
Регулярные выпуски «РМЖ» №27 от 25.12.2005 стр. 1880
Рубрика: Общие статьи
Авторы: Шостак Н.А. 1 , Аничков Д.А. 1 ФГБОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России, Москва, Россия
Для цитирования:
Шостак Н.А., Аничков Д.А. Метаболический синдром и подагра – подходы к антигипертензивной терапии. РМЖ. 2005;27:1880.
Введение Метаболический синдром (МС) представляет собой совокупность сердечно–сосудистых факторов риска, объединенную общим патогенетическим механизмом, резистентностью периферических тканей к инсулину [1]. Основными компонентами МС являются артериальная гипертензия, абдоминальное ожирение, снижение холестерина липопротеидов высокой плотности (ХС ЛПВП), гипертриглицеридемия и гипергликемия натощак [2]. В то же время нарушения обмена мочевой кислоты, изменения системы гемостаза, эндотелиальная дисфункция, повышение уровня С–реактивного белка и недостаточное снижение АД в ночной период часто сопутствуют МС [3]. Указанные аномалии имеют патогенетическое, клиническое и в некоторых случаях – прогностическое значение. Так, недостаточное снижение АД в ночные часы ассоциируется с поражением органов–мишеней и увеличением риска сердечно–сосудистых событий у больных с артериальной гипертензией [4]. Поэтому нормализацию суточного ритма АД у больных МС можно рассматривать как дополнительную цель антигипертензивной терапии [5].
Метаболический синдром (МС) представляет собой совокупность сердечно–сосудистых факторов риска, объединенную общим патогенетическим механизмом, резистентностью периферических тканей к инсулину [1]. Основными компонентами МС являются артериальная гипертензия, абдоминальное ожирение, снижение холестерина липопротеидов высокой плотности (ХС ЛПВП), гипертриглицеридемия и гипергликемия натощак [2]. В то же время нарушения обмена мочевой кислоты, изменения системы гемостаза, эндотелиальная дисфункция, повышение уровня С–реактивного белка и недостаточное снижение АД в ночной период часто сопутствуют МС [3]. Указанные аномалии имеют патогенетическое, клиническое и в некоторых случаях – прогностическое значение. Так, недостаточное снижение АД в ночные часы ассоциируется с поражением органов–мишеней и увеличением риска сердечно–сосудистых событий у больных с артериальной гипертензией [4]. Поэтому нормализацию суточного ритма АД у больных МС можно рассматривать как дополнительную цель антигипертензивной терапии [5]. Больные МС относятся к категории высокого риска сердечно–сосудистых осложнений [6]. В руководстве Европейского общества кардиологов/Европейского общества гипертензии и в 7 докладе Объединенного национального комитета США (JNC–7) пациентам с сахарным диабетом и МС рекомендованы все эффективные и хорошо переносимые антигипертензивные препараты, причем в JNC–7 сделан акцент в отношении диуретиков и b–блокаторов. Вместе с тем влияние различных антигипертензивных препаратов на показатели липидного, углеводного и пуринового обмена отличается. С этой точки зрения наиболее обоснованным представляется применение современных ингибиторов АПФ длительного действия (в частности, лизиноприла). Препарат обладает метаболической нейтральностью [7,8], а по некоторым данным даже повышает чувствительность тканей к инсулину [9]. Актуальным является изучение влияния лизиноприла на уровень мочевой кислоты у больных МС. Обоснованием являются результаты нескольких современных исследований. Гиперурикемия является фактором риска сердечно–сосудистой заболеваемости [10]. Высокий уровень мочевой кислоты повышает риск возникновения и прогрессирования артериальной гипертензии [11,12]. Уровень мочевой кислоты является мощным предиктором сердечно–сосудистой летальности у мужчин среднего возраста, даже после учета факторов, часто ассоциирующихся с метаболическим синдромом и/или подагрой [13]. Как бессимптомная гиперурикемия, так и подагра тесно связаны с инсулинорезистентностью и метаболическим синдромом. По данным P.H. Dessein et al. (2000), гиперинсулинемия наблюдается у 95% лиц с подагрой, метаболический синдром – у 76% [14]. Гиперурикемия тесно связана с гипертриглицеридемией [15]. Кроме того, гиперурикемия может служить суррогатным маркером синдрома инсулинорезистентности [16]. Возможная взаимосвязь между гиперурикемией и сосудистыми осложнениями артериальной гипертензии представлена на рисунке 1. Таким образом, целью настоящего исследования была оценка эффектов лизиноприла (Синоприла) и препарата сравнения атенолола на суточный профиль АД и влияния Синоприла на уровень мочевой кислоты у больных МС. Атенолол был выбран в связи с широким применением в клинике, известными гемодинамическими и метаболическими эффектами. Атенолол часто применяется как препарат сравнения в клинических исследованиях антигипертензивных препаратов [17,18]. Материал и методы Проведено открытое нерандомизированное сравнительное исследование в амбулаторных условиях. Критериями включения служили: мужской или женский пол; возраст от 30 до 60 лет; сочетание артериальной гипертензии I и II стадии по классификации ВОЗ 2003 г. [19] и двух других признаков метаболического синдрома по критериям ATP III [2]; информированное согласие. Пациенты исключались при наличии по меньшей мере одного из следующих критериев: вторичной артериальной гипертензии, сердечно–сосудистых событий в анамнезе, аритмий, декомпенсированного сахарного диабета, требующего лечения инсулином, экстремального ожирения (ИМТ>40 кг/м2), для женщин – период беременности или лактации. На этапе скрининга критериям включения соответствовал 41 пациент. Однако 3 больных отказались от участия в исследовании и 2 больных не закончили «отмывочный» период в связи с выраженным повышением АД. Таким образом, исследуемую группу составили 36 больных МС. После недельного вводного («отмывочного») периода пациентам в произвольном порядке назначали лизиноприл (Синоприл®, ЗАО «Фарм, Россия, совместно с Эджзаджибаши Фармасьютикал, Турция) 10 мг или атенолол 50 мг однократно утром. Продолжительность терапии составила 12 недель. Через 4 нед. проводили контроль АД и ЧСС, при недостаточной эффективности терапии дозу препарата (лизиноприла или атенолола) удваивали с сохранением однократного режима приема. Исходно и через 12 недель терапии проводили рутинное клиническое обследование, включающее измерение офисных значений АД и ЧСС; антропометрические измерения (рост, масса тела, окружность талии). Суточное мониторирование АД проводили с помощью приборов Meditech ABPM–04 и Schiller BR–102 с оценкой средних показателей систолического, диастолического АД и ЧСС, а также степени ночного снижения АД и ЧСС. Пациентам рекомендовали соблюдать обычный режим активности и вести дневник с указанием происходивших событий и времени ночного сна. Измерения проводились с интервалом 15 мин. днем и 30 мин. ночью. Исходное лабораторное обследование в группах Синоприла и атенолола включало оценку липидного профиля сыворотки: общего холестерина, триглицеридов, холестерина липопротеидов высокой плотности (ЛПВП) (энзиматический метод); сывороточной глюкозы натощак (окидазный метод). В группе лизиноприла все перечисленные параметры оценивали также через 12 недель терапии. Уровни мочевой кислоты, калия и креатинина оценивали исходно и через 12 недель терапии только в группе Синоприла. Основными критериями эффективности терапии были: изменение среднесуточных, среднедневных и средненочных показателей АД и ЧСС, степени ночного снижения АД и ЧСС, изменение уровня мочевой кислоты. Дополнительно учитывали долю пациентов, ответивших на терапию (responders rate), при этом критерием ответа было снижение офисного АД до целевых цифр 140/90 мм рт.ст. или более чем на 10% от исходного уровня. Безопасность терапии оценивали по наличию побочных эффектов (отсутствие побочных эффектов; побочные эффекты, не требующие отмены препарата; побочные эффекты, требующие отмены) и отсутствию неблагоприятной динамики лабораторных показателей (креатинин, калий). Статистическая обработка Статистический анализ проводили с помощью пакета программ Statistica 6.0 (StatSoft Inc., США). Для представления данных использовали методы описательной статистики (среднее, стандартное отклонение, медиана, квартили, абсолютные и относительные частоты). Для оценки вида распределения применяли визуальный анализ гистограмм распределения и критерий Шапиро–Уилка. Сравнение качественных данных проводили с помощью точного критерия Фишера, количественных (в случае нормального распределения) – с помощью критерия Стьюдента для связанных и несвязанных выборок. При распределении признака, отличающегося от нормального, применяли непараметрические методы (критерий Вилкоксона и Манна–Уитни). Уровень значимости был принят равным 0,05. Результаты Исходная характеристика больных в группах Синоприла и атенолола представлена в таблице 1. Статистически значимые различия между группами отсутствовали, за исключением показателей офисного диастолического АД и частоты пульса. Исходные показатели суточного мониторирования АД были сопоставимы, однако имелись различия среднесуточных и среднедневных показателей систолического АД и ЧСС (табл. 2). После назначения терапии, 1 больной в группе Синоприла были исключен из–за аллергической реакции (кожная сыпь). У 2 больных в группе атенолола препарат был отменен в связи с выраженной брадикардией. Таким образом, исследование закончили 23 больных в группе Синоприла и 10 больных в группе атенолола. Синоприл и атенолол в равной степени снизили среднесуточное систолическое и диастолическое АД (рис. 2). В то же время Синоприл в большей степени снижал систолическое АД в ночной период, в то время как атенолол – в дневной период (рис. 3). На фоне терапии атенололом наблюдалось ожидаемое снижение ЧСС (сутки: –13,6±1,8 уд./мин.; дневной период: –15,5±2,0 уд./мин., ночной период: –7,6±1,1 уд./мин., для всех показателей p Влияние исследуемых препаратов на суточный ритм АД и ЧСС представлено в таблице 3. В группе Синоприла не было значимых изменений степени ночного снижения АД, наблюдалась значимое (p=0,048) увеличение степени ночного снижения ЧСС. В группе атенолола отмечена тенденция к уменьшению степени ночного снижения систолического АД (p=0,093) и статистически значимое уменьшение степени ночного снижения ЧСС (p=0,022). Оба препарата продемонстрировали сходную эффективность в отношении офисного систолического и диастолического АД (–24±4/–14±2 мм рт.ст. в группе Синоприла и –21±6/–12±2 мм рт.ст., в группе атенолола; для всех показателей – p Данные о влиянии Синоприла на уровень мочевой кислоты, липиды сыворотки крови, креатинин и калий представлены в таблице 4. Влияние на уровень мочевой кислоты было положительным, но не достигло уровня статистической значимости. Наблюдалось повышение холестерина ЛПВП (p=0,018), остальные параметры существенно не изменились. Обсуждение Выбор антигипертензивного препарата у больного с гиперурикемией и/или подагрой и МС представляет большие сложности. Помимо высокой антигипертензивной эффективности и благоприятного влияния на характеристики суточного ритма АД и ЧСС, препарат не должен повышать уровень мочевой кислоты. Основные препараты, рекомендованные современными руководствами, так или иначе влияют на уровень мочевой кислоты в сыворотке крови. Так, терапия диуретиками сопровождается повышением мочевой кислоты, на фоне лечения b–блокаторами наблюдается тенденция к повышению; в то же время ингибиторы АПФ (например, лизиноприл) могут снижать уровень мочевой кислоты [20]. Следовательно, препаратом выбора в указанной группе больных может быть лизиноприл. По данным проведенного нами исследования, лизиноприл (Синоприл), как и препарат сравнения атенолол, эффективно снижает среднесуточное АД у больных МС. В то же время частота ответа на терапию (по данным офисных измерений АД) в группе Синоприла составила 79%, в группе атенолола – только 50%. Интересно отметить, что Синоприл в большей степени снижал ночное АД, в связи с чем наблюдались благоприятные изменения суточного ритма АД, в то время как атенолол ухудшал характеристики суточного циркадианного ритма АД. Полученные данные согласуются с результатами других исследователей, изучавших влияние лизиноприла и атенолола на показатели суточного ритма АД [8,21]. Обращает на себя внимание положительная динамика степени ночного снижения ЧСС в группе Синоприла и отрицательная – в группе атенолола. По данным литературы, недостаточное снижение ЧСС ночью ухудшает прогноз у больных с артериальной гипертензией [22]. Следовательно, полученные нами результаты могут иметь клиническое значение. Терапия Синоприлом привела к снижению уровня мочевой кислоты, не достигшего, однако, уровня статистической значимости. Препарат увеличил уровень холестерина ЛПВП, остальные показатели практически не изменились. Литературные данные о влиянии ингибиторов АПФ на уровень мочевой кислоты противоречивы. Так, в исследовании DeRosa et al. [23] сообщается об увеличении сывороточной концентрации мочевой кислоты у больных артериальной гипертензией на фоне 3–летней терапии эналаприлом. С другой стороны, есть данные о нивелировании лизиноприлом повышенного уровня мочевой кислоты, вызванного гидрохлоротиазидом [24]. Положительное влияние лизиноприла на сывороточный уровень мочевой кислоты обусловлено повышением урикозурии [20]. Таким образом, Синоприл обладает достоверным антигипертензивным эффектом (частота ответа 79%), характеризующимся нормализацией суточного профиля АД, увеличением степени ночного снижения ЧСС и АД, и оказывает благоприятное влияние на показатели липидного профиля (повышение ЛПВП) и показатели обмена мочевой кислоты. Выводы 1. Синоприл демонстрирует сопоставимое с атенололом влияние на показатели суточного мониторирования АД. 2. Характеристики суточного ритма АД под влиянием терапии Синоприлом не меняются, атенолол неблагоприятно влияет на суточный ритм систолического АД. 3. Синоприл, в противоположность атенололу, увеличивает степень ночного снижения ЧСС. 4. На фоне терапии Синоприлом наблюдается тенденция к снижению уровня мочевой кислоты и повышается уровень холестерина ЛПВП. Литература 1. Reaven GM. Metabolic syndrome. Pathophysiology and implications for management of cardiovascular disease. Circulation 2002;106:286–8 2. Grundy SM, Brewer Jr HB, Cleeman JI, et al. Definition of metabolic syndrome: report of the National Heart, Lung, and Blood Institute/American Heart Association conference on scientific issues related to definition. Circulation 2004;109:433–8 3. McFarlane SI, Banerji M, Sowers JR. Insulin resistance and cardiovascular disease. J Clin Endocrinol Metab 2001;86:713–8 4. Ohkubo T, Imai Y, Tsuji I. Prognostic significance of the nocturnal decline in blood pressure in individuals with and without high 24–h blood pressure: the Ohasama study. J Hypertens 2002;20:2183–2189. 5. Palatini P, Parati G. Modulation of 24–h blood pressure profiles: a new target for treatment? J Hypertens. 2005;23:1799–1801. 6. Lakka HM, Laaksonen DE, Lakka TA, et al. The metabolic syndrome and total and cardiovascular disease mortality in middle–aged men. JAMA 2002; 288:2709–16 7. Thurig C, Bohlen L, Schneider M, et al. Lisinopril is neutral to insulin sensitivity and serum lipoproteins in essential hypertensive patients. Eur J Clin Pharmacol 1995;49:21–6 8. Reisin E, Weir MR, Falkner B, et al. Lisinopril versus hydrochlorothiazide in obese hypertensive patients: a multicenter placebo–controlled trial. Treatment in Obese Patients With Hypertension (TROPHY) Study Group. Hypertension 1997;30(1pt 1):140–5 9. Fogari R, Zoppi A, Corradi L, et al. Comparative effects of lisinopril and losartan on insulin sensitivity in the treatment of non diabetic hypertensive patients. Br J Clin Pharmacol 1998;46:467–71 10. Wang JG, Staessen JA, Fagard RH, Birkenhager WH, Gong L, Liu L. Prognostic significance of serum creatinine and uric acid in older Chinese patients with isolated systolic hypertension. Hypertension 2001;37(4):1069–74. 11. Nagahama K, Inoue T, Iseki K, et al. Hyperuricemia as a predictor of hypertension in a screened cohort in Okinawa, Japan. Hypertens Res 2004;27:835–41 12. Sundstrom J, Sullivan L, D’Agostino RB, et al. Relations of serum uric acid to longitudinal blood pressure tracking and hypertension incidence. Hypertension 2005;45:28–33. 13. Niskanen LK, Laaksonen DE, Nyyssonen K, et al. Uric acid level as a risk factor for cardiovascular and all–cause mortality in middle–aged men: a prospective cohort study. Arch Intern Med 2004;164:1546–51. 14. Dessein PH, Shipton EA, Stanwix AE, et al. Beneficial effects of weight loss associated with moderate calorie/carbohydrate restriction, and increased proportional intake of protein and unsaturated fat on serum urate and lipoprotein levels in gout: a pilot study. Ann Rheum Dis 2000;59:539–43 15. Clausen JO, Borch–Johnsen K, Ibsen H, Pedersen O. Analysis of the relationship between fasting serum uric acid and the insulin sensitivity index in a population–based sample of 380 young healthy Caucasians. Eur J Endocrinol 1998;138:63–9 16. Fam AG. Gout, diet, and the insulin resistance syndrome. J Rheumatol 2002;29:1350–5. 17. UK Prospective Diabetes Study Group. Efficacy of atenolol and captopril in reducing risk of macrovascular and microvascular complications in type 2 diabetes: UKPDS 39. BMJ 1998;317:713–20. 18. Dahlof B, Devereux RB, Kjeldsen SE, et al. Cardiovascular morbidity and mortality in the losartan intervention for endpoint reduction in hypertension study (LIFE): a randomised trial against atenolol. Lancet 2002;359:995–1003. 19. 2003 World Health Organization (WHO)/International Society of Hypertension (ISH) statement on management of hypertension. J Hypertens. 2003;21(11):1983–92. 20. Reyes AJ. Cardiovascular drugs and serum uric acid. Cardiovasc Drugs Ther. 2003;17(5–6):397–414 21. Munakata M, Imai Y, Hashimoto J, et al. The influence of antihypertensive agents on circadian rhythms of blood pressure and heart rate in patients with essential hypertension. Tohoku J Exp Med. 1992;166(2):217–27 22. Verdecchia P, Schillaci G, Borgioni C, et al. Adverse prognostic value of a blunted circadian rhythm of heart rate in essential hypertension. J Hypertens 1998;16:1335–43. 23. De Rosa ML, Cardace P, Rossi M, Baiano A, de Cristofaro A. Comparative effects of chronic ACE inhibition and AT1 receptor blocked losartan on cardiac hypertrophy and renal function in hypertensive patients. J Hum Hypertens. 2002;16(2):133–40. 24. Leonetti G. Comparison of metabolic and hemodynamic effects of hydrochlorothiazide in monotherapy and in association with lisinopril. An Italian multicenter study. Minerva Cardioangiol. 1995;43(9):389–98
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Поделитесь статьей в социальных сетях
Порекомендуйте статью вашим коллегам