Наш эксперт
Марина Поздеева
Город: Днепропетровск
Провизор первой категории и заведующая аптекой. Автор многочисленных работ по фармакологии и фармакотерапии
Неутешительные статистические отчеты свидетельствуют, что почти у 80–90 % людей в возрасте старше 65 лет есть рентгенологические признаки остеоартроза [1]. Это заболевание нередко долгие годы протекает скрыто, а затем обрушивается на человека с безудержной силой. Каковы способы его медикаментозного контроля и может ли помочь фармацевт покупателю, страдающему остеоартрозом суставов?
Сложности определения
Понятие «остеоартроз» не так просто, как кажется. Под ним понимают не одну патологию, а целую группу дегенеративных заболеваний суставов, имеющих схожие проявления. «Точкой приложения» остеоартроза служат, как правило, крупные суставы, на которые приходится основная нагрузка: коленные, бедренные, плечевые, суставы пояснично-крестцового отдела. Иногда в патологический процесс вовлекаются и более мелкие суставы кистей рук. Искореженные пальцы пожилых людей, бросающиеся в глаза при одном лишь беглом взгляде, — яркий признак прогрессирующего остеоартроза.
При локальном течении заболевания поражаются один-два, а при генерализованном — сразу три или более суставов. В первом случае чаще всего развивается остеоартроз коленных суставов — гонартроз. Именно он входит в число основных причин инвалидизации в России [2]. Кстати, женщины страдают гонартрозом чаще мужчин: гендерное соотношение составляет 1,7:1 в «женскую пользу» [1]. И вообще, слабому полу с остеоартрозом «повезло» гораздо больше, чем сильному. Женщины лидируют среди больных старше 55 лет, а тяжелое течение заболевания — эрозивный остеоартроз — встречается у них в 12 раз чаще, чем у мужчин [1].
Факторы риска
Специалисты различают первичный, или идиопатический, остеоартроз, причина которого остается неустановленной, и вторичный, развивающийся в силу известных факторов риска.
Один из основных факторов — возраст. Известно, что распространенность остеоартроза критически возрастает среди лиц старше 50 лет. Врачи связывают эту тенденцию с неизбежными возрастными изменениями в синтезе основных стройматериалов костной, хрящевой и соединительной ткани коллагена и протеогликанов, приводящими к снижению предела прочности суставного хряща и уменьшению содержания в нем питательных веществ. Более склонны к развитию остеоартроза и тучные люди, страдающие повышенным весом или ожирением, — чем выше масса тела, тем большая нагрузка приходится на несущие суставы.
К факторам риска относятся также травмы, в том числе и в далеком прошлом, мышечная слабость, инфекционные заболевания, некоторые заболевания крови (например, серповидноклеточная анемия), сахарный диабет, генетические нарушения метаболизма, воспалительные артрозы. Повышается вероятность развития заболевания остеоартроз у женщин с низким уровнем эстрогенов, чем отчасти и объясняется «половая несправедливость» в пожилом возрасте. Вносят свой негативный вклад в здоровье суставов и условия труда. Регулярные тяжелые физические нагрузки тоже не проходят даром, оставляя «разрушительный» след на хрящах и крупных суставах.
Патогенез: как это происходит?
Первый явный признак заболевания — боль. Как правило, она сопровождается снижением амплитуды движений и появлением хруста в суставах. Во время или после отдыха, в том числе и ночного, у больных появляется скованность суставов, которая проходит через полчаса после восстановления активности.
Долгое время остеоартроз суставов считался исключительно дегенеративным расстройством, характеризующимся биохимическим распадом хряща. Однако сегодня уже не вызывает сомнений, что в патологический процесс вовлекается и костная, и соединительная ткани, причем немаловажную роль в нем играет воспаление.
Заболевание начинается с повышения синтеза основного компонента соединительной ткани — протеогликанов, приводящего к отеку хряща. Эта стадия может продолжаться на протяжении многих лет, причем нередко без каких‑либо клинических проявлений. Иногда больной с удивлением замечает лишь некоторую припухлость сустава, но зачастую не придает ей значения. А между тем остеоартроз набирает обороты: постепенно изменяется качественный состав протеогликанов и самого хряща, развиваются необратимые биохимические изменения, способствующие дальнейшей регенерации и хрящевой, и костной ткани.
В ходе развития заболевания увеличивается выброс в ткани и провоспалительных медиаторов, запускающих воспалительную реакцию. Кроме того, вследствие хронического воспаления происходит так называемый ангиогенез — процесс создания дополнительной сети кровеносных сосудов, который дополнительно активирует воспаление. В конечном счете на поверхности хряща образуются вертикальные расселины и трещины, он теряет эластичность и функциональность. В тяжелых случаях функция хряща полностью нарушается, что сопровождается нарушением подвижности сустава. Наиболее неблагоприятен прогноз течения остеоартроза у пожилых людей с высоким индексом массы тела, особенно если в патологический процесс вовлечены сразу несколько суставов.
НПВС
Наиболее эффективными препаратами для лечения артроза являются нестероидные противовоспалительные средства. Парацетамол – препарат выбора для лечения артроза коленного сустава и других локализаций у пациентов с умеренным болевым синдромом. Согласно европейским рекомендациям (ESCISIT), суточная доза парацетамола для постоянного приёма равна 2-4 г. В российских рекомендациях, более приближенных к реальным клиническим условиям, рекомендуемая на постоянный приём доза препарата не должна превышать 2 грамма в сутки. В указанной дозе парацетамол можно безопасно принимать для лечения артроза в течение двух лет. При применении более высоких доз препарата, особенно у пожилых пациентов, существенно повышается частота нежелательных реакций.
Для лечения пациентов с артрозом врачи Юсуповской больницы применяют следующие НПВС:
- ацетилсалициловую кислоту – длительность действия от 4 до 6 часов, разовая доза варьирует в пределах от 500 до 1000мг, высшая суточная доза составляет 3000мг;
- ибупрофен – продолжительность действия 6-8 часов, разовая доза равна 200-400мг, суточная – 2400мг;
- диклофенак – действует в течение 8-12 часов, разовая доза составляет 50-100мг, уточная – не должна превышать 150мг;
- индометацин – длительность действия от 6 до12 часов, разовая доза находится в пределах 200-400мг, высшая суточная – 2400мг;
- напроксен – применяется по 250-1000мг за один приём, но не больше 1200мг в сутки, действует 12 часов.
Неселективные НПВС при длительном лечении артроза могут оказывать выраженное побочное действие. При высоком риске развития осложнений врачи Юсуповской больницы для лечения артроза применяют селективные ингибиторы ЦОГ-2: мелоксикам по 7,5- 15мг 1 раз в сутки, нимесулид по 100-200мг 2 раза в сутки, целекоксиб по 100-400 мг 1 раз в сутки. Для лечения остеоартрита НПВС применяют только в период усиления болей в минимально эффективных дозах.
Клинические проявления остеоартроза
Начальным проявлением остеоартроза служит боль. Как правило, она сопровождается снижением амплитуды движений и появлением хруста в суставах. Во время или после отдыха, в том числе и ночного, у больных появляется скованность суставов, которая проходит самостоятельно через полчаса после восстановления активности. Утренняя скованность характерна и еще для одного заболевания, ревматоидного артрита, но она длится дольше, чем при остеоартрозе — час и даже более.
Остеоартроз пальцев рук чаще развивается у женщин, уродуя фаланги пальцев. На них появляются узлы Гебердена — патологические наросты, при этом в большинстве случаев воспалительные изменения, которые сопровождаются выраженной болью, остаются маловыраженными или вовсе незамеченными.
Диагностика остеоартроза не вызывает затруднений — самая обычная рентгенограмма, как правило, прекрасно визуализирует разрушительные процессы в суставах и хрящах. И тогда дело за лечением.
Нестероидные противовоспалительные препараты при остеохондрозе
Нестероидные противовоспалительные препараты (НПВП) или средства (НПВС) – это группа лекарственных веществ, которые обладают обезболивающими, противовоспалительными и жаропонижающими свойствами. Термин «нестероидные» в названии медикаментов указывает на их отличие от глюкокортикоидов, которые параллельно с вышеуказанными качествами несут в себе массу нежелательных побочных эффектов, присущих стероидам.
Первое противовоспалительное вещество было получено из коры ивы в 1829 году, это была салициловая кислота. На тот момент главными обезболивающими препаратами считались опиаты, которые вызывали быстрое привыкание, угнетали психику и дыхательные функции, обладали седативными качествами.
С тех пор нестероидные средства прочно заняли свои позиции в медицинской практике при лечении заболеваний, проявляющихся мышечными болями, лихорадкой, воспалением и подобными состояниями. Современная медицина значительно расширила список нестероидных противовоспалительных препаратов, которые сочетают в себе высокую эффективность, улучшенную переносимость и минимум побочных эффектов. Кроме того, большую часть подобных лекарств можно приобрести в аптечных сетях по достаточно доступным ценам без рецепта доктора.
При болях в спине, остеохондрозе, радикулите, люмбалгии, невралгиях и прочих заболеваниях опорно-двигательного аппарата НПВП используются для устранения болевых ощущений, снятия спазмированности и воспаления мягких тканей, что позволяет частично восстановить двигательные возможности пациента. При этом следует помнить, что противовоспалительные средства только купируют боль, но не являются лекарством от основного заболевания.
Механизм воздействия
Основным и главным элементом воздействия НПВС является ингибирование (подавление) синтеза (выработки) простагландинов из арахидоновой кислоты. Простагландины – медиаторы воспалительных реакций, которые провоцируют локальное расширение сосудистого русла в очаге патологии, отек, спазм, экссудацию, миграцию лейкоцитов и прочие явления.
Другие биологически активные качества препаратов:
- сенсибилизация (повышение чувствительности) рецепторов к медиаторам боли и механическим воздействиям, путем снижения порога болевой чувствительности;
- повышение чувствительности клеток гипоталамуса головного мозга, которые отвечают за терморегуляцию, к воздействию эндогенных пирогенов, образующихся в организме человека при попадании в него болезнетворных вирусов, микробов, токсинов и пр.
Менее выраженные механизмы воздействия:
- торможение окисления липидов;
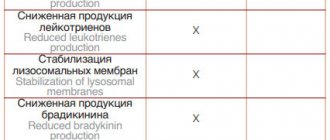
- стабилизация лизосомных мембран, что предупреждает разрушение клеточных структур;
- снижение синтеза АТФ;
- затормаживание выработки ревматоидных факторов;
- нарушение или ослабление проведения болевых импульсов по нервным волокнам спинного мозга и т.д.
Классификация НПВС
Нестероидные противовоспалительные препараты подразделяются по активности основного воздействия и химическому составу:
- Препараты с ярко выраженными противовоспалительными качествами:
- группа салицилатов (аспирин, дифлунизал);
- группа пиразолидинов (фенилбутазон);
- группа оксикамов (пироксикам, мелоксикам);
- группа производных индолуксусной кислоты (индометацин, сулиндак);
- группа производных фенилуксусной кислоты (диклофенак);
- группа производных пропионовой кислоты (ибупрофен, напроксен).
- Препараты с некислотными производными:
- группа алканонов (набуметон);
- группа производных сульфонамида (нимесулид, целекоксиб).
- Препараты со слабо выраженными противовоспалительными качествами, но с ярким анальгезирующим и жаропонижающим эффекетом:
- группа пиразолонов (метамизол, аминофеназон);
- группа производных парааминофенола (парацетамол);
- группа производных антраниловой кислоты (мефенаминовая кислота);
- группа производных гетероарилуксусной кислоты (кеторолак).
При этом по нарастанию противовоспалительного воздействия на организм человека, лекарственные препараты можно расставить в следующем порядке: аспирин, амидопирин, ибупрофен, напроксен, кетопрофен, пироксикам, диклофенак, флурбипрофен, индометацин.
По нарастанию анальгезирующих качеств: аспирин, ибупрофен, напроксен, пироксикам, амидопирин, флурбипрофен, индометацин, диклофенак натрия, кетопрофен, кеторолак.
Показания к применению
Нестероидные противовоспалительные средства рекомендуется использовать для лечения хронических и острых заболеваний, связанных с возникновением воспаления, болевого синдрома, повышения температуры.
Наиболее часто НПВС назначаются при:
- остеохондрозе, спондилезе и других дегенеративно-дистрофических патологиях скелета;
- остеопорозе, остеопатии, компрессионных переломах тел позвонков, патологических переломах костей конечностей;
- искривлениях осанки на поздних стадиях, после оперативного вмешательства в структуры позвоночника или травматических повреждений спины;
- миозитах, радикулите, ишиасе, люмбалгии, невритах и невралгии;
- ревматоидном артрите, остеоартрите, подагре, воспалительных артропатиях и пр.;
- опухолях и метастазах в костных структурах, сопровождающихся болью;
- головных болях, мигрени или лихорадке.
Противопоказания
Несмотря на все положительные качества противовоспалительных препаратов, не стоит забывать, что и они имеют определенные побочные эффекты. Наиболее часто они связаны с пищеварительным трактом и почками (так как большинство НПВС являются кислотами), а именно:
- язвенная болезнь желудка или двенадцатиперстной кишки;
- гастриты или эрозивное воспаление слизистых оболочек желудочно-кишечного тракта;
- желудочно-кишечные кровотечения;
- диспепсия, диарея;
- тошнота и рвота;
- нарушения деятельности печени и почек, нефрит, нефротический синдром, острая почечная недостаточность, что чревато задержкой натрия и воды в тканях организма и развитием артериальной гипертензии или сердечной недостаточности.
Кроме того, препараты аспириновой группы противопоказаны детям до 12 лет, аспирин и индометацин вызывают приступы бронхиальной астмы. Со стороны сердечно-сосудистой системы возможно нарушение свертываемости крови, цитопения, инфаркт миокарда, инсульт, тромбоз периферических сосудов и прочие нарушения.
Гораздо реже при лечении противовоспалительными лекарствами наблюдаются:
- головокружения, головные боли, спутанность сознания, нарушения координации движений;
- фотодерматиты или фотосенсибилизация (повышенная чувствительность кожи и слизистых оболочек к ультрафиолетовым или другим лучам);
- нарушения ферментации;
- аллергическая реакция или другие высыпания на коже;
- бессонница, повышенная возбудимость, нервозность.
Список основных препаратов, используемых при остеохондрозе
Индометацин. Рекомендуется для системного применения при лечении остеохондроза, остеоартрита, спондилита, подагры, ревматизма, болей в позвоночнике и прочих заболеваний. Принимается в виде таблеток, капсул во время или после еды, ректальных свечей в дозировке 25-50 мг 2-3 раза в сутки, но не более 200 мг. Может оказывать побочное воздействие на желудочно-кишечный тракт и нервную систему (головокружение, депрессия, шум в ушах, нарушение зрительных функций).
Ибупрофен. Применяется при радикулитах, артрозах, деформирующем остеоартрозе, анкилозирующем спондилите, подагре, бурсите, инфекционно-воспалительных заболеваниях структур скелета. Выпускается в виде гелей, мазей, таблеток, капсул, ампул, суппозиториев. Назначается по 0,4-0,8 г 3-4 раза в сутки после еды для лечения заболеваний опорно-двигательного аппарата. Для устранения болевого синдрома, при травмах мягких тканей или растяжении связок – 1,2-2,4 г в сутки, разделенных на несколько приемов. Может вызывать изжогу, диарею, тошноту, головокружения, аллергические реакции и пр.
Диклофенак. Используется для посттравматического лечения суставов и мягких тканей, мышечных болевых синдромов, отечности и воспалений, ревматических и неревматических мышечных болей. Выпускается в виде таблеток различной дозировки, покрытых оболочкой и растворяющихся в желудке, растворов для инъекций, ректальных свечей, гелей и мазей различной концентрации. Суточная доза при приеме внутрь не должна превышать 150 мг, для 1% геля – 2-4 г, 5% геля – 2 г. Местной реакцией на применение лекарства может быть зуд, покраснение, экзема, фотосенсибилизация, шелушение, системной – отек Клинке, бронхоспазм, крапивница, гастрит, язва.
Кетонал. Средство предназначено для симптоматической терапии дегенеративно-дистрофических заболеваний скелета, а также для снятия болевых синдромов различной этиологии. Таблеточная форма препарата назначается для приема внутрь после еды, запивая водой или молоком (не менее 100 мл), в дозировке 150-200 мг, разделенных на 2 приема. Можно чередовать употребление: утром – в виде таблеток, вечером – в виде ректальных суппозиториев. Побочные эффекты: тошнота, рвота, диарея, метеоризмы, головокружения, сонливость, быстрая утомляемость, нервозность, аллергические реакции.
Мовалис. Прописывается в острый начальный период для лечения или краткосрочными курсами для устранения симптомов артритов, остеохондроза, спондилита, ревматизма и прочих поражений опорно-двигательного аппарата. Выпускается в виде гелей, мазей, таблеток, покрытых оболочкой, ампул, суппозиториев. Препарат принимается во время еды, запивая достаточным количеством воды в дозировке 7,5-15 мг/сут, допускается комбинирование различных форм вещества (таблетки, свечи, уколы), но суточная доза не должна превышать 15 мг. Нежелательные последствия, иногда вызываемые лекарством: изменение состава крови, сонливость, дезориентация, колит, гастрит, язва, перфорация ЖКТ, нефрит, повышение артериального давления, одышка, аллергия.
Пироксикам. Рекомендуется для лечения воспалительных и дегенеративно-дистрофических заболеваний суставов и позвоночника, болевого синдрома и отечности сухожилий, мышц, суставов, после перенапряжения, травм, хирургических операций, инфекционно-воспалительных поражений тканей организма. Принимается внутрь после еды, запивая достаточным количеством воды в дозе 20-40 мг, разделенных на 1-2 приема в сутки. В числе побочных эффектов могут возникать: слабость, бессонница, депрессия, сухость во рту, стоматит, отрыжка, запоры, учащенное сердцебиение, скачки артериального давления и прочие проявления.
Автор: К.М.Н., академик РАМТН М.А. Бобырь
Как лечить остеоартроз? Основные задачи терапии
Лечение остеоартроза — комплексный процесс. Наряду с фармакотерапией в него должны входить и немедикаментозные способы контроля. Не стоит приуменьшать важность лечебной гимнастики, физиотерапии и даже трудотерапии. Немалую роль играет и уменьшение нагрузки на несущие суставы. При остеоартрозе терапия должна включать в себя весь перечень мер.
Сказать, что заболевание легко поддается коррекции, нельзя. Даже наоборот: лечение остеоартроза суставов — длительный, непростой и комплексный процесс. Наряду с фармакотерапией в него должны входить и немедикаментозные способы контроля. Больные, страдающие повышенной массой тела, должны приложить максимум усилий для ее нормализации. Не стоит приуменьшать важность лечебной гимнастики, физиотерапии и даже трудотерапии. Немалую роль играет и уменьшение нагрузки на несущие суставы, к примеру, коленные и бедренные.
Фармакотерапевтический контроль над течением остеоартроза основан на применении нескольких групп лекарственных препаратов.
Анилиды
Единственный современный представитель этой группы, парацетамол, как ни странно, входит в перечень препаратов, которые применяют для уменьшения выраженности болевого синдрома при остеоартрозе. Доказано, что парацетамол оказывает умеренное анальгетическое действие и может использоваться в соответствии с рекомендуемой дозировкой и длительностью курса.
Нестероидные противовоспалительные препараты — НПВП
При остеоартрозе применяют наружные формы (мази, гели, пластыри, суппозитории), пероральные (таблетки, капсулы), а также парентеральные. НПВП ингибируют фермент циклооксигеназу (ЦОГ), подавляя выработку медиаторов воспаления, которые ответственны и за болевой синдром, и за развитие воспалительного процесса. Следует помнить, что прием пероральных и инъекционных неселективных НПВП — кетопрофена, ибупрофена, мелоксикама, диклофенака, напроксена и некоторых других — может привести к развитию НПВП-ассоциированных гастропатий. Во избежание подобных побочных эффектов больным, страдающим желудочно-кишечными заболеваниями, НПВП назначают «под прикрытием» ингибиторов протонного насоса (например, омепразола). Кроме того, в целях безопасности, приоритет имеют местные средства: если они эффективно купируют боль и воспаление, к внутренним лекарственным формам стараются не прибегать.
Наряду с неселективными НПВП при остеоартрозе могут использоваться и селективные средства, ингибирующие только целевую ЦОГ-2, — коксибы (целекоксиб).
Местные анальгетики
Особое место в местной терапии остеоартроза занимают препараты, содержащие капсаицин. Это синтетический аналог природного соединения, которое обнаружено в горьком перце. Исследования доказали, что капсаицин неплохо справляется с болевым синдромом при остеоартрозе. Поэтому авторитетные международные организации, занимающиеся проблемами дегенеративных заболеваний суставов, включили капсаицин в список средств, рекомендованных для лечения остеоартроза.
В отечественных аптеках капсаицин продается в форме пластыря, который накладывают на самые болезненные участки кожи.
Другие препараты
В качестве ненаркотических анальгетических средств для уменьшения выраженности боли применяют диацереин. Он также доказал умеренный обезболивающий эффект. Кроме того, диацереин признан более безопасным средством, чем НПВП. Отметим, что один из самых неприятных побочных эффектов при его применении — диарея.
При тяжелом болевом синдроме врачи могут прибегать к назначению наркотических анальгетиков, в частности, трамадола. В случае выраженного прогрессирования заболевания назначают и внутрисуставные инъекции глюкокортикостероидов.
Нестероидные противовоспалительные препараты при лечении заболеваний суставов
Для цитирования. Имаметдинова Г.Р., Чичасова Н.В. Нестероидные противовоспалительные препараты при лечении заболеваний суставов // РМЖ. 2015. No 25. С. 1491–1495.
Заболевания опорно-двигательного аппарата являются одной из самых частых причин обращения пациентов к врачу. Широкая распространенность в популяции, многолетнее персистирование боли и воспаления, неуклонное прогрессирование, быстрое развитие инвалидизации, ухудшение качества жизни, уменьшение ее продолжительности, а также значительный экономический ущерб для больных и общества определяют не только клиническую, но и социальную значимость хронических заболеваний опорно-двигательного аппарата [1–3]. Основными симптомами заболеваний опорно-двигательного аппарата являются боль и воспаление. В большинстве случаев боль в различных структурах опорно-двигательного аппарата носит хронический характер, а наиболее частая причина ее развития – хроническое воспаление в синовиальной оболочке. Длительное персистирование боли и воспаления неизменно приводит к деструкции суставов и утрате функции опорно-двигательного аппарата. Лечение хронической боли и воспаления является сложной задачей, требует проведения многолетней комплексной противовоспалительной терапии, одним из компонентов которой являются нестероидные противовоспалительные препараты (НПВП). НПВП относятся к числу наиболее широко применяемых в клинической практике лекарственных препаратов [4]. Их использует примерно каждый 4-й человек на планете, каждый 3-й – в возрасте старше 60 лет [5]. Хорошо известно, что основным механизмом действия НПВП является подавление активности циклооксигеназы (ЦОГ) [6]. При этом большинство положительных эффектов НПВП (подавление воспаления, боли, лихорадки) связаны с подавлением активности ЦОГ-2, а побочных реакций – с подавлением активности ЦОГ-1 [7–9]. По механизму действия НПВП разделяют на неселективно подавляющие активность ЦОГ-1 и ЦОГ-2 (н–НПВП) и селективно подавляющие активность ЦОГ-2 (с–НПВП). С-НПВП эффективны в лечении боли и воспаления при более низкой частоте развития побочных реакций по сравнению с н-НПВП. Подавление ЦОГ-1 обусловливает широкий спектр побочных реакций н-НПВП. Наиболее частым является поражение желудочно-кишечного тракта (ЖКТ) (НПВП-гастропатия) [10, 11], что нередко становится основанием для прерывания лечения. Следует подчеркнуть отсутствие связи между субъективными побочными эффектами и эндоскопически выявляемыми язвами и тяжелыми ЖКТ-осложнениями. Так, в 58–80% случаев язвы на фоне анальгетического эффекта НПВП бессимптомны [12]. Однако клиницисты должны четко выделять факторы риска развития тяжелых осложнений со стороны ЖКТ – язвенного кровотечения и сердечно-сосудистой системы (ССС): инфаркта миокарда, инсульта. В 2015 г. опубликованы новые клинические рекомендации «Рациональное применение нестероидных противовоспалительных препаратов в клинической практике», подготовленные Ассоциацией ревматологов России, Российским обществом по изучению боли, Российской гастроэнтерологической ассоциацией, Российским кардиологическим обществом, Ассоциацией травматологов-ортопедов России [13]. Совместное обсуждение на экспертном совете выработало единый подход к выделению факторов риска нежелательных явлений со стороны ЖКТ и ССС. Основные положения, представленные в рекомендациях, включают: структурированный подход к назначению НПВП, стратификацию сердечно-сосудистых факторов риска, алгоритм назначения НПВП. Алгоритм назначения НПВП в соответствии с рекомендациями представлен в таблице 1. Согласно этим рекомендациям, с-НПВП показаны при умеренном риске кардиоваскулярных осложнений и умеренном и высоком риске ЖКТ-осложнений.
Известно, что н-НПВП отрицательно влияют на хрящ и утяжеляют течение артроза, оказывают негативное влияние на функцию печени и почек, а у больных, имеющих сопутствующие заболевания бронхов, могут вызывать бронхоспазм, усугублять течение бронхиальной астмы. В последние годы появляются все новые данные о частоте сопутствующей патологии у пациентов с заболеваниями опорно-двигательного аппарата. Необходимость в противовоспалительной терапии, подчас длительной, чаще возникает у лиц пожилого возраста, как правило, имеющих коморбидные состояния и сопутствующую им терапию. По мнению многих авторов [14–17], наиболее частыми коморбидными состояниями являются артериальная гипертензия (АГ), ишемическая болезнь сердца (ИБС), сахарный диабет, патология ЖКТ. С одной стороны, это факторы риска непереносимости НПВП, а с другой стороны, прием НПВП усугубляет течение АГ, застойной сердечной недостаточности, уменьшает эффективность антигипертензивной терапии [18–22]. Таким образом, препарат для лечения хронической боли и воспаления должен обладать не только высокой эффективностью, но и хорошим профилем безопасности. В этом плане интерес представляет селективный ингибитор ЦОГ-2 нимесулид, который уже около 30 лет с успехом используют врачи разных специальностей. По своему анальгетическому, противовоспалительному и жаропонижающему действию нимесулид не уступает н-НПВП, а по некоторым данным, даже несколько их превосходит [23]. Результаты целого ряда исследований in vitro и ex vivo свидетельствуют, что нимесулид более селективно ингибирует ЦОГ-2, чем ЦОГ-1 [24–28] (рис. 1).
В терапевтических концентрациях нимесулид ингибирует 88% активности ЦОГ-2 и 45% активности ЦОГ-1 [29]. При этом если воздействие на ЦОГ-1 прекращается по истечении 24 ч, то воздействие на ЦОГ-2 продолжается намного дольше [30], и это различие сохраняется при длительном применении [31]. Этот своеобразный механизм действия объясняет низкое число осложнений со стороны ЖКТ. Весьма интересным является тот факт, что низкую частоту поражения ЖКТ на фоне лечения нимесулидом связывают не только с ЦОГ-2 селективностью препарата, но и с антигистаминным действием, приводящим к снижению секреции соляной кислоты в желудке [32]. Также установлено, что нимесулид обладает способностью ингибировать интерлейкин-1β (IL–1β) в культуре синовиальных фибробластов [33]. Имеются данные о том, что наряду с ингибицией ЦОГ нимесулид обладает целым рядом ЦОГ-независимых механизмов, среди которых особенно важное значение имеет его способность ингибировать апоптоз хондроцитов [34]. Кроме того, препарат и его метаболиты проявляют непосредственно антиоксидантную активность в отношении различных свободных радикалов [35]. Нимесулид снижает дегрануляцию протеогликанов, угнетает активность эластазы, коллагеназы, стромелизина, подавляет гиперальгезию, индуцированную брадикинином и фактором некроза опухоли-α (ФНО-α) [25, 27, 36]. Препарат способен подавлять активность провоспалительных цитокинов: интерлейкина-6, ФНО-α, металлопротеиназ, фермента фосфодиэстеразы IV, активирующего макрофагальную и нейтрофильную активность [25, 37, 38]. Короткий период полувыведения (1,8–4,7 ч), быстрое достижение максимальной концентрации в плазме крови и синовиальной жидкости обусловливает высокую скорость наступления анальгетического эффекта и уменьшение частоты побочных эффектов нимесулида. При пероральном приеме препарат быстро и практически полностью абсорбируется независимо от приема пищи. Благодаря своим биохимическим свойствам нимесулид легко попадает в очаг воспаления. Концентрация свободного нимесулида непосредственно в очаге воспаления (особенно в ткани сустава), где рН среды более низкий, может быть намного выше его плазменной концентрации [39, 40]. Результаты исследований, проведенных отечественными и зарубежными авторами, подтверждают высокую эффективность нимесулида при лечении острой [41, 42] и хронической боли. Так, показано, что эффективность нимесулида была сопоставима с эффективностью диклофенака [43] и напроксена [44] у больных остеоартрозом (ОА) и ревматоидным артритом (РА) [44, 45]. Оценке безопасности нимесулида посвящен целый ряд краткосрочных и пролонгированных исследований. По данным мировой литературы, частота побочных явлений при лечении нимесулидом колеблется в пределах 6,8–36% с четкой зависимостью от дозы и длительности приема препарата. В частности, при анализе результатов нескольких клинических исследований, включавших 22 938 больных ОА, пролеченных нимесулидом в дозе 100–400 мг в течение 5–21 сут (в среднем 12 сут), общая частота побочных реакций составила 8,2% [47]. По данным другого многоцентрового исследования, в котором участвовали 12 607 пациентов с различными ревматическими и ортопедическими заболеваниями, на фоне лечения нимесулидом 400–200 мг/сут в течение 21 сут частота развития побочных эффектов составила 6,8% [48]. Как свидетельствуют результаты многочисленных исследований, проведенных отечественными и зарубежными авторами, нимесулид характеризуется хорошей переносимостью в отношении ЖКТ. Так, Kriegel W. et al. проводили сравнительное исследование 370 больных ОА, получавших нимесулид 200 мг/сут и напроксен 750 мг/сут в течение 12 мес. Эффективность обоих препаратов оказалась сопоставимой, а общее число лекарственных осложнений при использовании нимесулида в сравнении с напроксеном оказалось ниже: 47,5 и 54,5% соответственно [44]. Особого внимания заслуживают исследования, проводящиеся в условиях реальной клинической практики. Bradbury F. представил данные о частоте ЖКТ-осложнений при использовании диклофенака, нимесулида и ибупрофена. Суммарная частота поражения ЖКТ при использовании нимесулида была достоверно ниже по сравнению с таковой диклофенака (12,1%) и не отличалась от таковой ибупрофена – 8,1% и 8,6% соответственно [49]. Отечественными авторами была проведена оценка безопасности применения нимесулида в реальной клинической практике у 322 больных ревматическими заболеваниями, получавших нимесулид в суточной дозе 200 мг длительные сроки (12 мес.). Ни у кого из этих больных не было серьезных осложнений со стороны ЖКТ – кровотечения или перфорации язвы. Язвы желудка и двенадцатиперстной кишки (ДПК) были обнаружены у 13,3% больных [50]. Данные, полученные в ходе ранее проведенного эндоскопического исследования 4931 больных, получавших н-НПВП, продемонстрировали более высокую частоту развития язв верхних отделов ЖКТ – 18,1% больных [51] (рис. 2). Следует обратить внимание на данные популяционного исследования, в котором проводилась оценка риска развития ЖКТ-кровотечения на фоне приема различных НПВП. Было показано, что относительный риск развития кровотечения для нимесулида составил 3,2, для диклофенака – 3,7, мелоксикама – 5,7 [52]. Результаты эндоскопического исследования, проведенного А.Е. Каратеевым, продемонстрировали, что при использовании нимесулида поражение верхних отделов ЖКТ возникало значительно реже, чем при применении диклофенака, кетопрофена, индометацина – суммарное число язв желудка и ДПК составило 4,4% и 14,6% соответственно [53]. При анализе 10 608 спонтанных сообщений о серьезных побочных эффектах НПВП за период 1988–2000 гг., проведенном итальянскими учеными [54], оказалось, что частота побочных реакций со стороны ЖКТ на фоне приема нимесулида была в 2 раза ниже, чем на фоне препаратов сравнения (рис. 3).
Большой интерес представляют исследования безопасности применения нимесулида в высокой суточной дозе. Так, применение нимесулида в суточной дозе 400 мг у больных РА продемонстрировало не только высокую эффективность, но и хорошую переносимость препарата [55]. Позднее отечественными авторами было проведено многоцентровое исследование эффективности и безопасности нимесулида в суточных дозах 200 и 400 мг в сравнении с диклофенаком 100 и 200 мг/сут в течение 4-х нед. с ЭГДС-контролем при раннем РА. Результаты исследования продемонстрировали, что эффективность нимесулида была несколько выше, чем диклофенака, а развитие язв и множественных эрозий желудка или ДПК на фоне приема нимесулида было достоверно ниже, чем у больных, принимавших диклофенак, – 1,3% и 5,9% соответственно [45]. Совсем недавно были опубликованы результаты популяционного исследования, проведенного итальянскими учеными. Оценивался риск развития НПВП-ассоциированных осложнений со стороны ЖКТ у 588 827 пациентов при 3 623 341 назначений различных НПВП за период с 2001 по 2008 г. Следует особо подчеркнуть, что низкий риск развития серьезных ЖКТ-осложнений на фоне приема нимесулида был сопоставим с таковым у целекоксиба [56]. Аспекты кардиоваскулярной безопасности с-НПВП широко обсуждаются в мировой литературе. По результатам анализа, проведенного А. Helin-Salmivaara еt al., значение относительного риска инфаркта миокарда для нимесулида составило 1,69, что не превышало суммарного риска для всего класса [57]. По данным отечественных авторов, из 322 больных РА инфаркт миокарда был зафиксирован у 1 мужчины 68 лет с длительным анамнезом ИБС и АГ. Стойкое повышение АД отмечено у 11,5% больных, у 2 больных с наличием высокой степени риска АГ в анамнезе была выявлена отрицательная динамика на ЭКГ [50]. Следует отметить, что в исследованиях, проведенных зарубежными авторами (результаты которых упоминались выше), значимого повышения частоты кардиоваскулярных осложнений на фоне приема нимесулида не отмечалось [43, 44]. Вопросы гепатотоксичности нимесулида многократно обсуждались медицинской общественностью на протяжении нескольких последних лет. Анализ литературных данных свидетельствует о том, что гепатотоксичность нимесулида не выше, чем у других НПВП [58]. При кратковременном использовании нимесулида (не более 30 дней) повышение АЛТ и АСТ в 2 и более раз отмечается лишь у 0,4% больных, а при длительном (более 6 мес.) – частота подобных изменений не превышает 1,5% [59, 60]. У 322 больных, получавших нимесулид в течение 12 мес., не было выявлено ни одного случая развития клинических симптомов поражения печени (желтухи, гепатомегалии, симптомов печеночной недостаточности). Повышение уровня печеночных трансаминаз (АСТ, АЛТ) более чем в 2 раза было зарегистрировано в 7 случаях (2,2%) у больных РА, получавших еще и метотрексат и лефлуномид [50]. В самом крупном популяционном исследовании гепатотоксичности нимесулида [61] представлен анализ частоты лекарственного поражения печени у 397 537 пациентов, получавших различные НПВП за период 1997–2001 гг. Было показано, что нимесулид вызывал гепатопатии в 35,5 случая на 100 тыс. пациентов, что значительно реже, чем диклофенак – 39,2 и ибупрофен – 44,6. По данным испанских исследователей [62], за 10-летний период применения нимесулида серьезные гепатотоксические осложнения развивались крайне редко (рис. 4). Интересны результаты, полученные отечественными авторами в ходе изучения влияния нимесулида на функцию печени при лечении подагрического артрита. Как известно, пациенты с подагрой зачастую имеют метаболические нарушения и высокую частоту злоупотребления алкоголем, что повышает риск развития побочных реакций со стороны печени. Однако на фоне использования нимесулида в дозах до 400 мг/сут отсутствовала отрицательная динамика биохимических показателей крови, свидетельствующих о поражении печеночных клеток или холестазе [63].
Результаты метаанализа за 10-летний период (с 1988 по 1997 г.) продемонстрировали, что на 100 тыс. пациентов, принимавших нимесулид, отмечено только 11 случаев возможной связи почечных осложнений с приемом препарата, из которых только в 4-х проводилась монотерапия нимесулидом [64]. Установлено, что нимесулид крайне редко вызывает усиление бронхоспазма у больных, страдающих бронхиальной астмой и гиперчувствительностью к ацетилсалициловой кислоте или другим НПВП, поскольку не обладает перекрестной реактивностью с ацетилсалициловой кислотой и н-НПВП в отношении индукции обострения астмы и является одним из препаратов выбора (среди с-НПВП) у этих больных [25, 65]. Как уже упоминалось, экспериментальные данные продемонстрировали отсутствие у нимесулида отрицательного действия на хрящ [33, 34]. Несколько позже W. Kullch et al. в пилотном клиническом исследовании отметили положительное влияние нимесулида на течение ОА тазобедренных и коленных суставов [66]. Результаты научных исследований и большой клинический опыт применения нимесулида свидетельствуют о его высокой анальгетической и противовоспалительной активности и хорошей переносимости. Все вышесказанное послужило основанием для появления целого ряда дженериков этого препарата. Недавно в России появился новый дженерик нимесулида – Немулекс® в виде гранул для приготовления суспензии. Такая лекарственная форма препарата обеспечивает более быстрое наступление клинического эффекта по сравнению с таблетированной формой. Отличительной особенностью Немулекса является отсутствие в его составе высококалорийного полисахарида мальтодекстрина, что позволяет назначать препарат пациентам с СД, избыточной массой тела, нарушением обмена веществ. К настоящему времени уже имеются данные о результатах открытых проспективных краткосрочных (10–15 дней) клинических исследований препарата в суточной дозе 200 мг в ревматологической и неврологической практике [67–69]. Так, положительный эффект препарата Немулекс® в отношении основных клинических проявлений анкилозирующего спондилита у 30 больных продемонстрирован в исследовании НАУТИЛУС. По данным авторов, клинически значимого улучшения достигли 60% пациентов, при этом выраженность боли в спине уменьшилась в 2 раза. Побочные реакции включали повышение АСТ, АЛТ у 10% пациентов (купировались в течение 1 нед. на фоне диеты и назначения гепатопротекторов) и диспетические проявления у 10% пациентов (без наличия эрозивных изменений ЖКТ при проведении ЭГДС-контроля) [67]. Еще одно исследование было посвящено оценке эффективности и безопасности препарата Немулекс® в сравнении с диклофенаком, индометацином у 30 больных ОА. По данным авторов, эффективность всех препаратов была сопоставимой и не различалась статистически. Однако при использовании Немулекса анальгетический эффект развивался примерно на 2 дня раньше, чем у препаратов сравнения. Побочные эффекты на фоне приема Немулекса отмечались у 4 пациентов (13% случаев). У 3 больных имели место диспептические расстройства, у 1 – подъем АД. Побочные реакции были слабо выражены и не требовали отмены препарата [68]. По данным Д.И. Лахина, у 30 больных ОА через 15 дней лечения отмечены исчезновение признаков синовита, достоверное уменьшение боли (с 69,3±0,74 до 21±0,29), а также улучшение функции суставов у всех пациентов. Среди побочных реакций фигурировали только признаки гастропатии у 2 (6,7%) пациентов (при наличии в анамнезе язвенной болезни желудка). По мнению подавляющего большинства пациентов (23 человека – 76,6%), переносимость лечения была хорошей, у 7 (23,3%) – удовлетворительной [69]. В амбулаторных условиях проведено исследование, включавшее 49 пациентов с дорсопатией. Все пациенты получали комплексное лечение, включающее Немулекс® и Хондрогард. Через 15 дней большинство пациентов (29 человек – 59,5%) отметили исчезновение болей в спине. 2 пациента (4%) отметили появление дискомфорта в эпигастрии, что привело к самостоятельной отмене препарата. При этом, по данным автора, контрольная ЭГДС патологических изменений не выявила [72]. Таким образом, результаты исследований показали, что Немулекс® обладает отчетливым анальгетическим и противовоспалительным свойствами в сочетании с хорошей переносимостью. Тем не менее, учитывая короткие сроки и небольшое количество исследований, целесообразно изучить эффективность и безопасность препарата в более длительные сроки на различных когортах пациентов.
Корректоры метаболизма костной ткани в лечении остеоартроза
Отдельных слов заслуживает группа препаратов, корректирующих метаболизм костной ткани. К ним относятся хондропротекторы глюкозамин, хондроитина сульфат, а также ризедроновая кислота. Последняя чаще применяется при остеопорозе — она ингибирует резорбцию костей. Популярностью среди клиентов аптек пользуются и комбинированные препараты, содержащие комплекс хондроитина сульфата и глюкозамина. Иногда в качестве дополнительного обезболивающего и противовоспалительного компонента к ним присоединяется ибупрофен.
Хондропротекторы стимулируют регенерацию костной ткани, оказывают противовоспалительное и обезболивающее действие. Таблетированные и наружные формы (например, хондроитина сульфат в капсулах, таблетках или мази, а также комплексные средства) относятся к безрецептурным препаратам. А значит, когда за рекомендацией в аптеку приходит клиент, страдающий остеоартрозом, провизор вправе расширить консультацию и посоветовать не только наружные или внутренние НПВП из ОТС-группы, но и хондропротекторы, защищающие хрящ от дальнейшего повреждения.