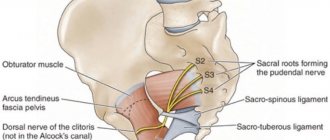
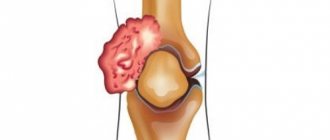
Ревматоидный артрит – это так называемое системное заболевание, которое поражает соединительную ткань организма, что влечет за собой массу негативных последствий. Сильно страдают небольшие суставы, которые разрушаются, меняют свои размеры и форму. Около 1% людей во всем мире страдает этой болезнью.
Сложность в том, что точных причин болезни пока никто не знает. Есть только комплекс моментов, которые способствуют развитию заболевания, поэтому и избежать его нельзя. Сама же болезнь приводит к утрате трудоспособности человека, сильно снижает качество его жизни.
Выявляют ревматоидный артрит в среднем в 30-35 лет, потом болезнь постепенно развивается и к пожилому возрасту максимально влияет на жизнь человека. Женщины страдают этим недугом в 3 раза чаще, чем мужчины.
Возможные причины проблемы
Медицинское сообщество предполагает, что на развитие болезни влияет сразу много факторов, а не какой-то один. К возможным причинам ревматоидного артрита относят:
- генетическую предрасположенность. Речь о том, что у человека на генетическом уровне заложена склонность к разным нарушениям в развитии иммунитета;
- некоторые возбудители инфекций. Тут есть несколько «кандидатов», но до конца исследователи этой проблемы пока не определились;
- совокупность спусковых механизмов: переохлаждения, гиперинсоляция, интоксикация, бактериальные инфекции, прием некоторых лекарств. К этой же группе относят нарушения работы щитовидной железы и даже стрессы.
Есть информация о том, что кормление грудью в течение двух лет – это фактор, который уменьшает риск появления заболевания (в среднем в два раза).
Профилактика артрита
Чтобы предупредить развитие артрита и новые рецидивы, рекомендуется придерживаться следующих правил:
- ограничивайте нагрузки на колени во время работы или занятий спортом, отдавая предпочтение тренировкам, не нагружающим коленные суставы;
- постепенно снижайте лишний вес;
- избегайте длительного статического напряжения, переохлаждения и перегрузок;
- вовремя лечите травмы, растяжения, разрывы связок и инфекционно-воспалительные заболевания;
- проводите разминку перед каждой тренировкой, используя ходьбу и упражнения на растягивание мышц передней и задней групп бедра.
Наверх к содержанию
Информация в данной статье носит справочный характер и не заменяет профессиональной консультации врача. Для постановки диагноза и назначения лечения обратитесь к квалифицированному специалисту.
Симптомы
К симптомам ревматоидного артрита относят:
- скованность в утреннее время. То есть во время пробуждения и в течение часа после сна человек не может двигаться активно, в привычном для себя режиме – бывает сложно выполнить даже простые действия, например, переложить подушку, одеяло;
- боли в суставах, которые могут повторяться с разной периодичностью. Если суставы прощупывать, то боль усиливается. При развитии болезни проявляется сниженная подвижность суставов. Температура кожи в области сгибов может быть выше, чем на остальных участках кожи;
- наличие ревматоидных узелков. Плотные подкожные образования прощупываются в области суставов;
- общее плохое самочувствие. Оно может проявляться снижением аппетита, беспричинной потерей веса, постоянным чувством усталости.
При агрессивном течении заболевания и длительном периоде болезни могут повреждаться другие внутренние органы, что встречается не так часто.
У вас появились симптомы ревматоидного артрита?
Точно диагностировать заболевание может только врач. Не откладывайте консультацию — позвоните по телефону
Лечение посттравматического артрита
Процесс лечения посттравматического артрита подразумевает сочетание ряда методов, среди которых:
- фармакологические;
- физиотерапевтические;
- немедикаментозные.
Своевременное начало лечения позволяет достигнуть ремиссию.
Грамотно выстроенное лечение посттравматического артрита обеспечивает возможность:
- предотвращение прогресса патологии;
- купирование боли и снижение воспаления;
- возможность сохранения подвижности сустава;
- сохранение прежнего уровня жизни.
Курс, его продолжительность и перечень дополнительной, поддерживающей терапии определяется исключительно лечащим врачом, в индивидуальном порядке, с учетом степени развития патологического процесса, возраста и состояния здоровья пациента.
Физиотерапия
Физиотерапевтическое лечение является эффективным методом восстановления функциональных возможностей организма человека при различных по типу заболеваниях и патологиях.
Наиболее эффективными признаны:
Препараты, используемые в лечении посттравматического артрита
Медикаментозное лечение предполагает реализацию нескольких этапов:
- снятие острого воспалительного процесса;
- назначение поддерживающей терапии, предполагающей регенерацию суставных тканей и нормализацию обменных процессов.
В лечении травмы сустава используются НВПС (нестероидные противовоспалительные средства), к одним из самых эффективных среди которых принято относить «Артрадол»
. Препараты этой группы играют важнейшую роль в успешности лечения.
В зависимости от характера поражения, могут назначаться прочие группы препаратов, куда принято относить:
- обезболивающие;
- кортикостероиды;
- хондропротекторы.
Все назначаемые медикаментозные средства могут выпускаться в различных формах.
Лечебная физическая культура (ЛФК), как метод комплексного лечения посттравматического артрита
Лечебная физическая культура (ЛФК) является эффективной составляющей медикаментозного лечения, применение которого особо важно на этапе ремиссии.
Выполнение комплекса упражнений, разработанного в соответствии с имеющейся симптоматической картиной и общим состоянием здоровья пациента, способствует сохранению двигательной активности сустава, а также укреплению мышечного аппарата.
Гимнастические упражнения рекомендуется выполнять в различных положениях (сидя/лежа/в воде), под присмотром инструктора ЛФК.
Хирургическое вмешательство
Наличие запущенной стадии развития патологического процесса или отсутствие эффективности медикаментозного и физиотерапевтического лечения может привести к необходимости применения радикальных методов лечения
, среди которых – хирургическое вмешательство.
Проводятся операции двух типов:
- открытого;
- закрытого.
Реализует хирургическое вмешательство травматолог-хирург, после тщательно проведенного комплексного обследования, преимущественно под общим наркозом.
Пораженные суставы могут подвергаться таким манипуляциям, как:
- замена сустава эндопротезом;
- остеотомия (устранение деформации);
- остеосинтез (фиксация костных отломков) с использованием винтов, гвоздей, спиц и прочих медицинских конструкций;
- пластическая коррекция связочного аппарата.
Выписка пациента после операционных мероприятий, как правило, осуществляется после снятия швов.
Формы артрита
Заболевание в чистом виде предполагает, что поражаются только суставы, без воздействия на другие органы. Если речь о болезни с системными проявлениями, то в этом случае аутоиммунные процессы отражаются на сердце, легких, почках, нервной и других системах. Развитие заболевания связано с отложением в органах белка патологического типа.
Может выявить диагностика ревматоидного артрита и другие дополнительные заболевания. Он иногда сочетается с остеоартрозом, ревматизмом.
Есть и так называемый ювенильный вариант болезни – это тяжелая форма заболевания, которой страдают дети и подростки. Она тоже может захватывать только суставы или суставы вместе со внутренними органами.
Что такое посттравматический артрит?
Артрит
– это группа заболеваний, предполагающих поражение сустава дегенеративно-дистрофического типа. Патология может быть самостоятельным заболеванием или являться симптомом какого-либо другого.
Посттравматический артрит
– разновидность артрита, предполагающая развитие дегенеративно-дистрофических процессов на фоне перенесенной ранее травмы, в ситуации, когда наблюдается дисфункция поврежденной части тела.
Особо подверженными заболеванию принято считать спортсменов и людей преклонного возраста.
При отсутствии своевременной диагностики и необходимого лечения патология приводит к необратимой инвалидности пациента.
Разновидности болезни в зависимости от течения
Медленно прогрессирующий ревматоидный артрит предполагает, что болезнь развивается долгие годы, постепенно поражая суставы. Сами сочленения страдают не очень сильно. Здесь помогает лечение и можно сохранить довольно комфортный уровень жизни.
Быстро прогрессирующий тип характеризуется частыми и сильными обострениями, повреждения суставов сильные, лечение помогает слабо. Качество жизни человека ухудшается ощутимо.
Самый простой и легкий тип для пациента – болезнь без заметного прогрессирования. С ней можно прожить до глубокой старости, не особенно страдая от симптомов.
Причины посттравматического артрита
Прежде чем рассматривать симптомы посттравматического артрита, важно понимать причины его возникновения и развития.
Ключевая причина
посттравматического артрита – повреждение суставных тканей (мышечной, соединительной, костной), а также сосудов и нервов внутри них. Хрящевая ткань редко страдает от травмы, однако, расположенные около него воспалительные очаги провоцируют ускорение его износа.
Повреждения суставных тканей могут возникать вследствие таких причин, как:
- травмы, полученные в быту, на производстве или в ходе спортивной тренировки;
- повреждения, полученные в результате ДТП и при др. нестандартных ситуациях;
- операции и прочие медицинские мероприятия.
Кроме того, причинами посттравматического артрита не всегда являются серьезные повреждения. Патология может развиться на фоне отсутствия лечения даже легких ушибов.
Степени развития
От степени зависит то, насколько проявляется недостаточность опорно-двигательного аппарата. Выделяют 4 ступени с учетом нулевой:
- нулевая. Пациент самостоятельно себя обслуживает, его жизнь практически не меняется;
- первая. За счет проблем с суставами пациенту доступны не все движения. Некоторые виды профессиональной деятельности уже исключены;
- вторая. На этой стадии человек утрачивает профессиональную трудоспособность;
- третья. Самая сложная степень предполагает, что у пациента нет возможности самостоятельно обслуживать себя даже в бытовом плане на сто процентов.
Очевидно, что при комбинации с другими заболеваниями ситуация на каждой стадии значительно осложняется.
Тяжелый вариант течения ревматоидного артрита
Течение РА весьма вариабельно. Это связано со многими причинами. Больной может оказаться резистентным к лечению либо не переносить его. Задержка с назначением терапии базисными противовоспалительными препаратами (БПВП) также ухудшает прогноз при РА. Кроме того, известно, что воспаление в синовиальной оболочке может начать развиваться задолго до появления первых клинических симптомов заболевания. Известно, что в крови больных РА за несколько лет до дебюта артрита (вплоть до 10 лет) выявляются серологические тесты, такие как ревматоидный фактор (РФ) и/или антитела к циклическому цитруллинированному пептиду (АЦЦП) [4] (рис. 1).
Морфологическое исследование синовиальной оболочки, полученной у больных в первые месяцы дебюта артрита, показало, что не у всех выявляются признаки острого ревматоидного воспаления, – у части больных уже в первом биоптате наблюдаются отчетливые признаки хронического синовита [5]. Именно у этих больных отмечался далее более торпидный вариант РА с плохим ответом на терапию БПВП. Тяжесть состояния больного РА на каждом этапе зависит от уровня воспалительной активности, что определяет выраженность болей в суставах, скованность, функциональные нарушения. При адекватно проводимой терапии и подавлении активности до развития необратимых анатомических изменений в суставах (деструкция, деформации) функция суставов восстанавливается (рис. 2). А тяжелый вариант течения болезни встречается при неадекватно проводимой или неэффективной терапии, определяется степенью стойкой утраты функциональной способности больного не только к профессиональному труду, но и к самообслуживанию. Поэтому как можно более раннее начало противовоспалительной терапии имеет при РА принципиальное значение.
В последнее десятилетие в практику здравоохранения внедрены диагностические критерии ранних стадий РА [6] для своевременного направления больного к ревматологу и раннего начала терапии. А появление новых классификационных критериев ACR/EULAR 2010 г. позволило как можно раньше начинать лечение БПВП [7]. Идеальным должно считаться начало терапии БПВП сразу после появления первых симптомов воспаления в синовиальной оболочке: утренней скованности, боли в суставах и припухлости, что и отражено в данных критериях: наличие полиартрита с вовлечением мелких суставов имеет наибольший вес. На практике больной с дебютом РА проходит подчас длинный путь консультаций, диагностических мероприятий до встречи с ревматологом.
Кроме того, начало болезни может быть клинически слабо выражено, и симптомы болезни медленно нарастают, что затрудняет установление диагноза РА. По данным зарубежных авторов [8] и по нашим данным [9], при остром дебюте РА отдаленный исход болезни лучше, чем при постепенном начале заболевания. Вероятно, острое начало болезни заставляет пациента быстрее обращаться за врачебной помощью, а врач в этом случае быстрее определяется с диагнозом и начинает терапию. Наши данные свидетельствуют о лучшем исходе РА, оцененном через 15 лет болезни по степени сохранности функции опорно-двигательного аппарата, выраженности деструкции в суставах, частоте многолетних ремиссий и выживаемости больных, при назначении БПВП в первые 6 мес. от дебюта симптомов артрита [10].
Задержка с назначением БПВП приводит к более плохому ответу на эти препараты, что было показано в контролируемых исследованиях [11]. Препаратом первой линии считается метотрексат, другие БПВП (лефлуномид, сульфасалазин) в начале лечения используют при невозможности назначить метотрексат. Терапия БПВП у многих больных приводит к подавлению активности и прогрессирования РА, особенно при назначении их в первые месяцы болезни. Но и начало терапии в очень ранний период болезни (1–2 мес. болезни) не во всех случаях позволяет добиться выраженного эффекта (клинической ремиссии или поддержания низкой активности РА). Во-первых, больной может не ответить на БПВП; во-вторых, у многих больных эффективность БПВП уменьшается через 1–2 года терапии, у части больных происходит последовательная смена базисных препаратов из-за симптомов непереносимости.
При неэффективности и/или непереносимости последовательно назначаемых БПВП и развивается тяжелая форма РА. Наиболее значимыми параметрами для определения тяжести РА являются выраженность деструктивных изменений в суставах и степень стойкой утраты функциональной способности суставов вплоть до утраты больным способности к самообслуживанию.
Большое количество рандомизированных клинических исследований (РКИ) было посвящено выявлению наиболее эффективных терапевтических стратегий в лечении больных РА: сравнивались результаты лечения при последовательной монотерапии БПВП, при их комбинации как в дебюте болезни (стратегия «step-down»), так и после присоединения 2-го, 3-го препаратов при неэффективности первого средства (стратегия «step-up»). В последних рекомендациях EULAR 2013 [12] использование комбинации БПВП предлагается и в дебюте лечения, что основывается на результатах нескольких рандомизированных открытых исследований [13–15].
Оценка в сравнительном аспекте эффективности монотерапии метотрексатом, сульфасалазином, антималярийными препаратами, циклоспорином А, лефлуномидом и их комбинаций [16–23] не показала однозначного преимущества комбинированной терапии БПВП перед их применением в виде монотерапии. В ряде исследований было показано, что через 6, 12 и 24 мес. клинический эффект был более выражен при использовании комбинации БПВП (либо при «step-up», либо при «step-down» стратегии) [19, 21, 24–28]; по данным других авторов [29, 30] не отмечено достоверных отличий во влиянии на показатели активности монотерапии или комбинации БПВП. При продлении срока исследований (до 5 лет) преимущества во влиянии на активность РА комбинации БПВП перед монотерапией не отмечено [16, 28, 29]. Оценка рентгенологических изменений в суставах через 1–2 года не показала преимуществ комбинированного лечения в исследовании MASCOT [21], а комбинация циклоспорина А и метотрексата в 2-х исследованиях через 6 [31] и 12 [32] мес. в большей степени подавляла прогрессирование деструкции, чем монотерапия метотрексатом. В исследовании FIN-RACo изменение счета Ларсена было достоверно меньше при использовании комбинации БПВП через 2 года [19], но через 5 лет достоверных различий между комбинированной терапией и монотерапией уже не отмечалось [20]. Следует отметить, что комбинация БПВП была более эффективна по сравнению с монотерапией различными БПВП только в том случае, если в комбинации использовался метотрексат.
Кроме того, интересные данные были получены при оценке эффективности двойных комбинаций БПВП с тройной комбинацией: сравнивали эффективность метотрексата + сульфасалазин, метотрексата + гидроксихлорохин и комбинации всех 3-х препаратов [13]. По критериям эффективности ACR было получено превосходство тройной комбинации над двойными, но только в группе больных, которые ранее не получали метотрексат. В группе больных, ранее лечившихся метотрексатом, эффект тройной комбинации не превышал эффект совместного применения метотрексата и гидроксихлорохина.
Весьма интересны данные, полученные в результате исследования TICORA [17, 33], которое сравнило результаты 18-месячного лечения 2-х групп больных РА: в 1-й группе лечение проводилось со строгим ежемесячным контролем изменения активности РА по DAS («tight» контроль), и в соответствии с динамикой DAS корригировалась терапия («интенсивная» группа). Во 2-й группе лечение проводилось рутинным способом без такого жесткого контроля. К концу исследования ремиссия была достигнута у 65% больных 1-й группы и только у 16% больных 2-й группы. Увеличение числа эрозий было меньше в 1-й группе. Контролируемое лечение («интенсивная» группа) сопровождалось более частой коррекцией терапевтической тактики (использование комбинации БПВП, эскалация их дозы, использование внутрисуставных введений ГК). Авторы при анализе этих результатов пришли к выводу, что контроль за лечением обеспечивает наилучшие результаты вне зависимости от выбора БПВП.
Такой же вывод сделан J.M. Albers et al. [34] при оценке результатов 4-х различных режимов использования БПВП: жесткий контроль за успешностью лечения обеспечивает сходные результаты терапии различными БПВП. При оценке лечения метотрексатом пациентов с ранним РА (длительность болезни <1 года) в исследовании CAMERA [22, 23] также сделан вывод, что строгий ежемесячный контроль динамики активности болезни («tight» контроль) и своевременная коррекция терапии позволяют добиться достоверно лучшего результата за период 2-летнего наблюдения. Так, в группе интенсивного контроля (n=76) частота ремиссий составила 50%, а при рутинном способе лечения (n=55) – 37% (p=0,03) [23]. Эти данные совпадают с нашим мнением, основанным на результатах более длительного открытого исследования эффективности базисной терапии у 240 больных: улучшение исхода РА (функциональное состояние суставов, рентгенологическая картина) зависит не только от сроков начала лечения, но и от степени обеспечения постоянного контроля за ходом лечения [10]. Также эти данные создали предпосылки для разработки современной стратегии лечения РА «Лечение до достижения цели» («Treat to target»), когда основной целью лечения становится достижение ремиссии, а альтернативной целью – достижение низкой активности РА [35].
Но даже при грамотном подходе к терапии больных РА в соответствии с внедренной в нашей стране стратегией лечения «Лечение до достижения цели» классическими БПВП (раннее начало терапии и постоянный контроль за степенью подавления активности и прогрессирования болезни) все же развивается тяжелая форма РА. По нашим данным и данным литературы, у 15–25% больных последовательно назначаемые БПВП не приводят к выраженному эффекту (хороший эффект по критериям EULAR или более чем 50% улучшение по критериям ACR) либо приводят к возникновению побочных реакций и необходимости отмены БПВП. Создание генно-инженерных биологических препаратов (ГИБП) позволило в значительной степени оптимизировать лечение больных РА.
В настоящий момент в Российской Федерации зарегистрированы 5 блокаторов фактора некроза опухоли-α (ФНО-α): инфликсимаб, адалимумаб, цертолизумаб пэгол, голимумаб, этанерцепт, препарат ритуксимаб, связывающий CD20, ингибитор растворимых мембранных рецепторов к интерлейкину-6 – тоцилизумаб и абатацепт. Все эти препараты продемонстрировали высокую эффективность у больных с недостаточным эффектом БПВП, включая метотрексат. Лечение ритуксимабом, как правило, проводится при неэффективности ингибиторов ФНО-α, хотя препарат может использоваться как первый ГИБП при особых показаниях (например, проживание в эндемичном по туберкулезу районе), что также отмечено в последних рекомендациях EULAR (2013) [12]. Остальные ГИБП могут быть первыми представителями этой группы, назначаемыми при отсутствии эффекта от БПВП.
С учетом высокой стоимости лечения ГИБП важным представляется вопрос отбора больных для терапии ГИБП. Как было показано в исследовании BEST [13], при неэффективности 2-х последовательно назначенных классических БПВП дальнейшее использование других БПВП не приводит к развитию эффекта. Поэтому во многих странах Европы и в России одним из критериев отбора больных для назначения ГИБП является неэффективность 2-х БПВП, одним из которых должен быть метотрексат. Как показывает анализ РКИ, начало терапии сразу с комбинации ГИБП и метотрексата не имеет преимуществ перед последовательным усилением терапии при недостаточном эффекте метотрексата [36]. Однако при наличии факторов неблагоприятного прогноза (высокая активность с вовлечением большого количества суставов, высокая концентрация РФ и АЦЦП, прогрессирование деструкции суставов) вопрос о применении ГИБП обсуждается после неэффективности первого БПВП.
Классические БПВП способны в дебюте РА оказать выраженное действие и подавить рентгенологическое прогрессирование деструкции у значительного количества пациентов. В нашей практике больным с установленным диагнозом РА сразу назначается метотрексат, при наличии противопоказаний индивидуально обсуждается выбор БПВП. Далее пациент наблюдается ежемесячно до выраженного эффекта с коррекцией терапии, проводимой индивидуализированно. В течение первых 3-х мес. лечения должно быть установлено, имеется ли эффект, какова его выраженность. Такой контроль за степенью подавления активности позволяет своевременно корректировать терапию, если это требуется. При 50% (и более) улучшении далее в течение первого года терапии оценивается, есть ли подавление прогрессирования эрозивного артрита. Недостаточный противовоспалительный эффект или появление новых эрозий в суставах кистей и стоп, развитие деструкции крупных суставов, сохранение внесуставных проявлений должны приводить к изменению терапии: увеличению дозы метотрексата или переходу на его подкожные инъекции, смене БПВП, комбинации БПВП или их комбинации с ГИБП. Увлечение симптоматической терапией, стремление подавить активность заболевания с помощью частых внутрисуставных или в/в введений глюкокортикоидов при отсутствии достаточного и стабильного эффекта БПВП не предупреждают развития тяжелой формы РА. Эти мероприятия могут быть только дополнением к лечению БПВП, но не подменять его.
Таким образом, для предупреждения утраты функции у больных РА, т. е. для предупреждения развития тяжелой формы болезни врач должен обеспечить следующее:
- раннее назначение БПВП всем больным РА;
- провести обучение больного с объяснением целей терапии, необходимости длительного (многомесячного и многолетнего) лечения, мониторинга переносимости препаратов;
- постоянный контроль за степенью подавления активности и прогрессирования болезни с объективной оценкой количественной выраженности суставного синдрома и деструктивных изменений в суставах, за переносимостью терапии;
- при неэффективности 2-х последовательно назначенных БПВП поставить вопрос о необходимости назначения ГИБП.
Для объективного контроля за активностью РА на каждом этапе лечения врач должен регистрировать число болезненных и припухших суставов, выраженность боли по оценке больным, общее состояние по оценке больным и врачом с использованием визуальной аналоговой шкалы, а также лабораторные параметры (СОЭ и С-реактивный белок). Контроль за успешностью терапии с использованием составного индекса DAS28 позволяет объективизировать контроль изменения активности РА.
Таким образом, внедрение новых классификационных критериев РА, наличие активных БПВП и арсенала ГИБП, безусловно, создает предпосылки для значимого улучшения исходов РА, сохранения качества жизни больных.
Литература
- Руководство по внутренним болезням. Гл. 9 / Р.М. Балабанова. М., 1997. С. 257–294.
- Goodson N., Symmons D. Rheumatoid arthritis in women: still associated with increased mortality // Ann. Rheum. Dis. 2002. Vol. 61. Р. 955–956.
- Riise T ., Jacobsen B.K., Gran J.T. et al. Total mortality is increased in rheumatoid arthritis. A 17-year prospective study // Clin. Rheum. 2002. Vol. 20. Р. 123–127.
- Nielen M.M., van Schaadenburg D., Reesnik HW. et al. Specific autoantibodies precede the symptoms of rheumatoid arthritis: A study of serial measurement in blood donors // Arthr. Rheum. 2004. Vol. 50. Р. 380–386.
- Шехтер А.Б., Крель А.А., Чичасова Н.В. Клинико-морфологические сопоставления при различных вариантах ревматоидного артрита (по данным пункционных биопсий синовиальной оболочки) // Терапевтический архив. 1985. № 8. С. 90–100.
- Emery P., Breedveld F., Dougados M. et al. Early referral recommendation for newly diagnosed rheumatoid arthritis: evidence based development of a clinical guide // Ann. Rheum. Dis. 2002. Vol. 61. Р. 290–297.
- Aletaha D., Neogi T., Siulman A.J. еt al. 2010 rheumatoid arthritis classification criteria: an Americam College of Rheumatology/European League Against Rheumatism collaborative initiativw // Ann Rheum Dis. 2010. Vol. 69. Р. 1580–1588.
- Zatarain E., Strand V. Monitoring disease stativity of rheumatoid arthritis in clinical practice: contributions from clinical trials // Nature Clinical Practice Rheumatology. 2006. Vol. 2. N 11. Р. 611–618.
- Чичасова Н.В. Лечение различных вариантов течения ревматоидного артрита // Москоский медицинский журнал. 1997. № 1. С. 21–26.
- Чичасова Н.В., Каневская М.З., Насонов Е.Л. и др. Исходы ревматоидного артрита при разных сроках начала терапии // Научно-практическая ревматология. 2010. № 3.
- Han C., Smolen J.S., Kavanaugh A. et al. Impact of disease duration and physical function on employment in RA and PsA patients // Arthr. Rheum. 2006. Vol. 54. Suppl. P. 54.
- Smolen J.S., Landewe R., Breedveld F.C. et al. EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs: 2013 update // Ann Rheum Dis. 2013 Oct 25. DOI: 10.1136/annrheumdis-2013-204573.
- O’Dell J.R., Leff R., Paulsen G. et al. Treatment of rheumatoid arthritis with methotrexate and hydroxichloroquine, methotrexate and sulphasalazine, or a combination of the three medications // Arthritis Rheum. 2002. Vol. 46. Р. 1164–1170.
- Saunders S.A., Capell H.A., Stirling A. et al. Triple therapy in early active rheumatoid arthritis. A randomized, single-blind, controlled trial comparing step-up and parallel treatment strategies // Arthritis Rheum. 2008. Vol. 58. Р. 1310–1317.
- De Jong P.H., Hazes J.M., Barrendregt P.J. et al. Randomized comparison of triple DMARD therapy with methotrexate monotherapy // Ann Rheum Dis. 2013. Vol. 72. Р. 72–78.
- Maillefert J.F., Combe B., Goupille P. еt al. Long-term structural effects of combination therapy in patients with early rheumatoid arthritis: five-year follow up of a prospective double blind controlled study // Ann. Rheum. Dis. 2003. Vol. 62. Р. 764–766.
- Grigor C., Capell H., Stirling A. et al. Effect of treatment strategy of tight control of rheumatoid arthritis (the TIСORA study): a single-blind randomised controlled trial // Lancet. 2004. Vol. 364. Р. 263–269.
- Goecor-Ruiterman Y.P., de Vries-Bouwstra J.K., Allaart C.F. et al. Clinical and radiographic outcomes of four different treatment strategies in patients with early rheumatoid arthritis (the BeST study): a randomised, controlled trial // Arthr. Rheum. 2005. Vol. 52. Р. 3381–3390.
- MottonenT., Hannonen P., Leirisalo-Repo M. et al. Comparison of combination therapy with single drug in early rheumatoid arthritis: a randomised trial. FIN-RACo Group // Lancet. 1999. Vol. 353. Р. 1568–1573.
- Korpela M., Laansonen L., Hannonen P. еt al. Retardation of joint damage in patients with early rheumatoid arthritis by initial aggressive treatment with disease-modifying antirheumatic drugs: five-year experience from FIN-RACo study // Arthr. Rheum. 2004. Vol. 50. Р. 2072–2081.
- Capell H., Madhok R., Porter D. et al. Combination therapy with sulphasalazine and methotrexate is more effective than either drug alone in rheumatoid arthritis (RA) patients with a suboptimal response to sulphasalazine: result from the double-blind placebo controlled MASCOT study // Ann. Rheum. Dis. 2007. Vol. 66. Р. 235–241.
- Bijlsma J.W., Weinblatt M.E. Optimal use of the methotrexate: the advantages of tight control // Ann. Rheum. Dis., 2007. Vol. 66. Р. 1409–1410.
- Verstappen S.M.M., Jacobs J.W., van der Veen M.J. et al. Intensive treatment with methotrexate in early rheumatoid arthritis: aiming for remission. Computer Assisted Management in Early Rheumatoid Arthritis (CAMERA, an open-label strategy trial) // Ann. Rheum. Dis. 2007. Vol. 66. Р. 1443–1449.
- Haagsma C.J., van Riel P.L., de Jong A.J., van de Putte L.B. Combination of sulphasalazine and methotrexate versus methotrexate alone: a randomised open clinical trial in rheumatoid arthrits patients resistant to suylphasalasine therapy // Dr. J. Rheum. 1994. Vol. 33. Р. 1049–1055.
- Dougados M., Combe B., Cantagrel A. еt al. Combination therapy in early rheumatoid arthritis: a randomised, controlled double-blind 52 week clinical trial of sulphasalazine and methotrexate with the single components // Ann. Rheum. Dos. 1999. Vol. 58. Р. 220–225.
- Stein M. et al. Combination treatment of severe rheumatoid arthritis with cyclosporine and methotrexate for forty-eight weeks. An open-label extension study // Arthr. Rheum. 1997. Vol. 40. Р. 1843–1851.
- Kremer J. et al. Concomitant leflunomide therapy in patients with active rheumatoid arthritis despite stable doses of methotrexate. A randomised, double-blind, placebo-controlled trial // Ann. Int. Med. 2003. Vol. 137. Р. 726–733.
- Kremer J. et al. Combination leflunomide and methotrexate therapy for patients with active rheumatoid arthritis failing methotrexate therapy: open label extension of a randomised, double-blind placebo controlled trial // J. Rheum. 2004. Vol. 31. Р. 1521–1531.
- Haagsma C.J., van Riel P.L., de Jong A.J., van de Putte L.B. Combination of sulphasalazine and methotrexate versus the single components in early rheumatoid arthritis: a randomsed, controlled, double-blind, 52 week clinical trial // Br. J. Rheum. 1997. Vol. 36. Р. 1082–1088.
- Hider S.L., Silman A.J., Bunn D. еt al. Comparing the long term clinical outcome between methotrexate and sulphasalazine prescribed as the first disease modifying antirheumatic drugs in patients with inflammatory polyarthritis // Ann. Rheum. Dis., published online 15 March 2006.
- Garards A. et al. Cyclosporine A monotherapy versus cyclosporine A and methotrexate combination therapy in patients with early rheumatoid arthritis: a double blind randomised placebo controlled trial // Ann. Rheum. Dis. 2003. Vol. 62. Р. 291–296.
- Marchesoni A. et al. Radiographic progression in early rheumatoid arthritis: a 12-month randomised controlled study comparing the combination of cyclosporine A and methotrexate with methotrexate alone // Rheum. 2003. Vol. 42. Р. 1545–1549.
- Porter D. Targeting persistent disease activity in early RA: a commentary on the TICORA trial // Int. J. Adv. Rheum. 2005. Vol. 3. Р. 2–6.
- Albers J.M., Paimela L., Kurki P. et al. Treatment strategy, disease activity, and outcome in four cohort of patients with early rheumatoid arthritis // Ann. Rheum. Dis. 2001. Vol.60. Р. 453–458.
- Smolen J.S., Aletaha D., Bijsma J.W. et al. For the T2T Expert Committee. Treating rheumatoid arthritis to target: recommendations of an international force // Ann Rheum Dis. 2010. Vol. 69. Р. 631–637.
- Насонов Е.Л., Каратеев Д.Е., Чичасова Н.В. Рекомендации EULAR по лечению ревматоидного артрита –общая характеристика и дискуссионные вопросы // Научно-практическая ревматология. 2013. № 51 (6). С. 609–622.
Диагностика
Для диагностики ревматоидного артрита используют разные методы:
- лабораторные. Они предполагают иммунологические, биохимические исследования и изучение общего анализа крови;
- инструментальные. Пункция сустава, радиоизотопное исследование, рентген – это распространенные варианты диагностики;
- биопсия. Она тоже относится к инструментальным, но вынесена отдельно, поскольку из всех перечисленных решений применяется наиболее редко.
Начинается диагностика с приема у врача и обследования. Для записи на консультацию необходимо обращаться к ревматологу.
Как быть?
Вместо них в меню нужно добавить молочные и рыбные блюда, гречку, фасоль, чечевицу, а также продукты, содержащие клетчатку и серу (семя льна, отруби, лук, чеснок). Они принимают активное участие в построении хрящевой и соединительной ткани.
Болят суставы? Ешьте меньше мяса
4. Ортопедическая обувь без назначения.
При артрозе голеностопного сустава, коленного или тазобедренного ортопеды часто рекомендуют носить ортопедические стельки, или супинаторы. Они поддерживают свод стопы и снижают нагрузку на суставы нижних конечностей. Это справедливо при условии правильного подбора. Если стельки выбраны наугад, они могут навредить.
Лечение в Москве
Для тех форм, когда лечение ревматоидного артрита может дать хороший результат, используют целый набор разных медикаментов:
- противовоспалительные нестероидные препараты;
- базисные препараты. Их изготавливают на основе нескольких действующих компонентов;
- гормональные вещества. В данном случае используют глюкокортикоиды в разных видах: таблетки, мази, средства для введения путем инъекций;
- биологические агенты: моноклональные антитела, регуляторы дифференцировки лимфоцитов и т.д.
Дополнительно к основному лечению пациентам предлагаются физиотерапевтические процедуры, прохождение лечебной гимнастики (только в момент ремиссии). Обязательно назначается профилактика остеопороза. А еще ревматоидный артрит, если он сильно снижает качество жизни, может предполагать хирургическую коррекцию «сложных» суставов.
Степени посттравматического артрита
Как и любой другой вид артрита, патология имеет несколько степеней развития:
1 степень
– небольшая скованность движений, дискомфорт пораженной части тела;
2 степень
– сужение суставной щели, образование костных наростов (остеофитов);
3 степень
– разрастание множественных остеофитов, полное отсутствие суставной щели.
Для каждой степени развития посттравматического артрита характерна определенная симптоматическая картина, позволяющая точно диагностировать степени прогресса патологии и сформировать наиболее эффективный план комплексного лечения пациента.
Профилактика осложнений
Если симптомы ревматоидного артрита были выявлены на ранней стадии, то своевременное лечение во многих ситуациях позволяет значительно затормозить патологические процессы и избежать осложнений. К эффективному лечению следует добавить и такие профилактические меры:
- ведение здорового образа жизни. Пациентам рекомендована и специальная диета;
- отказ от вредных привычек;
- регулярная физическая активность без чрезмерных нагрузок;
- повышенное внимание к лечению других заболеваний – даже обычных простуд.
Такая профилактика ревматоидного артрита дает хороший шанс на то, что человек сможет прожить жизнь в довольно комфортных условиях.
Вероятные осложнения посттравматического артрита
Несвоевременное обращение ко врачу, неточность диагностических мероприятий, а также отказ или отклонение от назначенного плана лечения может стать причиной развития нежелательных осложнений
, среди которых: