Знаменитая компания DePuy Synthes входит в огромный холдинг Johnson&Johnson. Основная специализация – производство инновационного и эффективного медицинского оборудование в сфере ортопедии, травматологии и хирургии.
Delta Motion
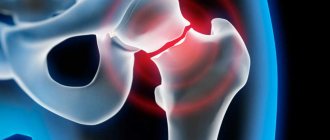
Компания DePuy стала основоположником производства приспособлений для протезирования в Соединенных Штатах Америки. Основана она была еще в конце девятнадцатого века. Специалисты компании на заре своей деятельности совершили настоящую революцию в лечение переломов шейки бедра. Они перестали применять деревянные приспособления, применявшиеся ранее для обездвиживания поврежденных конечностей. Им на смену пришли проволочные шины, которые оказались более эффективными.
Продукция компании
Корпорация DePuy производит и реализует сверхпрочные, надежные и современные медицинские изделия, которые применяются при лечении переломов, спортивных травм, эндопротезировании мелких и крупных суставов и так далее. Ассортимент продукции составляют следующие приспособления:
- протезы, применяющиеся для операций по тотальному эндопротезированию тазобедренных и коленных суставов;
- инструменты, применяющиеся при артроскопических хирургических операциях: фиксаторы и имплантаты;
- медицинские изделия, которые используются при проведении нейрохирургических операций: дрели, системы шунтирования, автоматизированные системы мониторинга и многое другое;
- системы для фиксации конечностей при травмах и переломах.
Подготовка к хирургическому вмешательству
В ходе подготовки к эндопротезированию будет проведен ряд исследований и анализов, чтобы подтвердить необходимость проведения операции и исключить возможные противопоказания. Также пациент проконсультируется с анестезиологом.
На приеме у хирурга будет подобран наиболее подходящий тип эндопротеза. Протез и методика протезирования подбираются в индивидуальном порядке, в зависимости от степени изношенности коленного сустава. Если поражена одна область сустава, то возможно проведение частичного (однополюсного) протезирования.
Как проходит операция?
Хирургическое вмешательство может быть выполнено либо под общим наркозом, либо под спинальной анестезией. Оно занимает обычно от одного до полутора часов. Доступ в коленный сустав осуществляется через короткий разрез кожи на внутренней стороне сустава. Изношенные суставные поверхности обрабатываются по специальной схеме таким образом, чтобы искусственный коленный сустав соответствующего размера мог быть хорошо припасован к кости.
Какие риски связаны с операцией такого рода?
К счастью, осложнения после такой операции бывают очень редко. Подготовка к операции проходит основательно, без спешки. Таким образом, риск и опасность осложнений сводятся к минимуму. Несмотря на все профилактические меры при проведении операции по эндопротезированию коленного сустава, как и при любой другой операции, существуют определенные риски, которые имеют место менее чем в 5% случаев. Применение хорошей хирургической техники и правильное обращение пациента с «новым коленом» после такой операции дают очень хорошие результаты. Благодаря замене коленного сустава вы можете снова наслаждаться жизнью без боли и больше двигаться. Однако не забудьте обращаться к врачу для регулярных осмотров в последующие годы!
Правила поведения, способствующие успеху операции
Ниже приведены некоторые важные правила поведения, способствующие успеху операции. Так, следует:
- после выписки из больницы продолжать выполнение выученных физиотерапевтических упражнений
- правильно наступать на стопу
- использовать костыли при ходьбе до момента достижения устойчивой ходьбы и нормальной походки
- соблюдать прямую походку с шагами равной длины
- использовать обувь со шнуровкой и мягкими, гибкими подошвами
Индивидуальный эндопротез Delta Motion
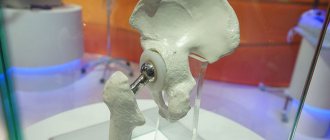
Приспособления для протезирования фирмы DePuy полностью соответствуют анатомической структуре поврежденного сустава, что позволяет в полном объеме восстановить двигательные функции после операции. Медицинские технологии и научные исследования не стоят на месте. Эндопротез Delta motion позволяет заменить пораженные участки сустава, при этом сохранив значительный объем костной массы.
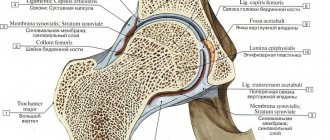
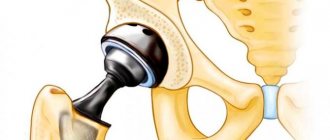
Смысл хирургического вмешательства заключается в установке специального медицинского имплантата, который состоит из трех компонентов:
- головки;
- ацетабулярной чашки с вкладышем;
- втулки.
Стержень протеза цементируется или запрессовывается в суставной впадине. Иногда для закрепления изделия используют винты и специальные фиксаторы. В некоторых других случаях при вживлении в организм эндопротез держится на связках и мышцах.
Средний срок эксплуатации современного эндопротеза составляет от пятнадцати до двадцати лет. По истечении этого срока старый протез заменяется новым при проведении повторной операции. Как правило, дата очередной проверки состояния имплантата назначается непосредственно лечащим врачом.
Протезы коленного сустава для тотального эндопротезирования
Zimmer — The NexGen® LPS-Flex Mobile Zimmer — LPS-Mobile Bearing Knees
- С подвижной платформой.
- Обе системы позволяют искусственному протезу коленного суставу сгибаться и свободно вращаться.
- Используются металлические компоненты: присоединяемый к концу бедренной кости, заменяющий верхнюю часть голени.
- Эндопротезы включают пластиковую суставную поверхность, свободно прикрепленную к опорной плите, выполняющую роль искусственного хряща.
- Обеспечивают 155⁰ активного сгибания и 25 градусов беспрепятственного внутреннего и внешнего вращения.
- Для фиксации используется костный цемент.
The Zimmer Gender Solutions® Patello-Femoral Joint
- Протезы коленного сустава с подвижной платформой.
- Предназначен для активных пациентов, позиционируется, как вариант раннего вмешательства.
- Позволяет сохранить большие участки костей, требует меньшего разреза.
- Использование данного имплантата требует от хирурга умения обращения со специальными инструментами, знание минимальноинвазивных техник.
- В эндопротезе учтены гендерные различия, специальная форма его компонентов более точно отражает особенности женской и мужской анатомии.
- Предполагает 35 различных вариантов проклейки.
DePuy Sigma® Rotating Platform Knees
- С подвижной платформой.
- Подразумевает установку подвижного подшипника, опирающегося на поворотную платформу, что позволяет имитировать естественные движения колена.
- Конструкция обеспечивает снижение внутреннего напряжения и износа, поэтому эксплуатируется он дольше, чем аналоги.
- По статистике, в мире имплантировано около 1 млн. подобных эндопротезов, 97% которых используются более 20 лет.
DePuy Sigma® Fixed-Bearing Knees
- Неподвижная опора.
- Используется износостойкий полиэтилен и передовые металлические компоненты, которые не вызывают отторжения в 99,6% случаев после 5 лет эксплуатации.
Smith & Nephew OXINIUM ®
- Неподвижная опора.
- Протез коленного сустава с высоким уровнем износостойкости.
- Изготавливается из металлического циркония, что делает его более стойким к истиранию и царапанью.
- При проведении испытаний было отмечено уменьшение износа полиэтилена на 85% по сравнению с кобальт-хромовыми материалами, используемыми в других имплантатах
Stryker Triathlon® Total Knee Replacement System
- Неподвижная опора.
- Этот тип искусственного сустава предназначен для работы с телом.
- Дает хорошие результаты по возврату двигательной активности после операции.
- Конструкция устройства позволяет имплантату сгибаться, расширяться, вращаться аналогично естественному колену
Biomet Vanguard® Complete Knee System
- Неподвижная опора.
- Устройство, подстраиваемое под конкретные особенности анатомии пациента.
- Предполагает высокую степень сгибания (около 145⁰).
- Доступен в 90 типоразмерах, 10 вариантах размеров бедренной кости.
Срок службы и материалы изготовления
На общий срок службы эндопротеза Delta Motion могут влиять различные факторы как по отдельности, так и в совокупности. На уменьшение или увеличение срока эксплуатации могут оказать влияние физическая активность больного, его возраст и вес, особенности строения костей, наличие хронических заболеваний, и, конечно же, материал, из которого изготовлен имплантат.
Чтобы устройство прослужило как можно дольше, к расходным материалам для его производства предъявляются самые высокие требования. Части протеза изготавливаются таким образом, чтобы уменьшить влияние трения, из-за которого компоненты быстро изнашиваются. Также немаловажную роль играет устойчивость к коррозийным процессам и иному негативному воздействию.
Самыми популярными расходниками при производстве протезов являются титановые или хромовые сплавы с применением базальта. Необходимая прочность и надежность достигается благодаря процессу горячей ковки. Втулки и головки протеза также изготавливаются из керамики, а вкладыши имеют в своем составе прочнейший полиэтилен.
Протезы коленного сустава для частичного эндопротезирования
BioMet Oxford ® Knee
- Устройство, предназначенное для пациентов с ограниченным (медиальным) артритом.
- В протезе используются подвижные пластиковые подшипники, имплантируется только с одной стороны.
- Позволяет удалять на 75% меньше костей и хрящей, поэтому процедура его установки менее болезненна, а скорость восстановления выше.
- Клинические испытания показывают 98% успеха после 10 лет ношения и 95% — после 15 лет
DuPuy Sigma® High Performance Partial Knee
- Предназначен для активных пациентов, для которых требуется высокая степень сгибания, но еще не наступило время полного эндопротезирования.
- Позволяет становиться на колени, приседать, сидеть со скрещенными ногами.
- Хирург использует любой из его компонентов по отдельности для замены нужного отсека колена.
- Сохраняет максимум неповрежденной площади родного колена.
ПОЛУЧИТЬ КОНСУЛЬТАЦИЮ ВРАЧА
Эндопротез Delta Motion: описание
Данная система представляет собой нецементированную чашку с вкладышем из высокопрочной керамики. Это является действительно новаторским решением, поскольку позволяет устанавливать протез молодым пациентам, чей организм плохо «уживается» с чужеродными объектами.
Структура Delta motion позволяет оптимизировать систему «головка-впадина», благодаря чему головки большего диаметра могут быть использованы в небольших вертлужных впадинах. В результате фиксация имплантата с суставом становится лучше, пациент может вести активную жизнь, прибегая к серьезным физическим нагрузкам.
Использование уникального протеза Delta motion позволяет стремительно реабилитироваться после операции и вернуться к полноценной жизни. Характеристики материала обеспечивают сохранность природной анатомии суставной массы; использование продукта будет полностью естественным.
Технология данной системы позволяет производить протезы, специально разработанные в соответствии с особенностями женских коленей. Они имеют более тонкую и менее объемную форму, что снижает нагрузку и обеспечивает естественность движений.
Основные виды операции по эндопротезированию коленного сустава
Говоря в целом, существует два основных варианта операции эндопротезирования коленного сустава:
- Одномыщелковое эндопротезирование
- Тотальное (полное) эндопротезирование
Одномыщелковый эндопротез замещает только часть изношенного сустава, поэтому данная операция показана пациентам с поражением одного мыщелка коленного сустава.
Тотальное эндопротезирование коленного сустава может быть классифицировано по признаку степени механической стабильности эндопротеза на:
Несвязанный
Полусвязанный
Анатомия протеза
По оценке аналитической компании GlobalData, к 2021 году объем мирового рынка тотального эндопротезирования тазобедренного сустава достигнет $7,1 млрд. При этом в 2014 году сумма судебных претензий к трем ведущим американским производителям имплантатов для этой операции достигла сопоставимой величины в $6 млрд. Причина в том, что американский регулятор FDA десятилетиями разрешал поставки эндопротезов без клинических исследований и, даже когда возникали проблемы, не спешил отзывать потенциально опасную продукцию с рынка.
GlobalData прогнозирует, что к 2021 году США с долей в 57% сохранят свое лидерство на рынке эндопротезирования бедренного сустава. Неудивительно, что большинство судебных тяжб с производителями эндопротезов тоже происходит в Америке.
Пара трения эндопротеза может изготавливаться из разных материалов: «керамика – керамика», «металл – полиэтилен», «керамика – полиэтилен», но большинство жалоб и претензий пациентов связано с ношением бедренных эндопротезов с парой трения «металл – металл».
Если на этапах разработки и производства такого эндопротеза были допущены ошибки, то при трении шара о чашку искусственного сустава образуется слишком много металлических микрочастиц, которые, попадая в окружающие сустав ткани, вызывают воспаление. Кроме того, стираясь, сустав становится нестабильным, человек начинает испытывать сильные боли и неудобство при ходьбе.
В 2012 году в одном из авторитетнейших медицинских журналов The Lancet было опубликовано исследование ученых из Бристольского университета. Они проанализировали данные Национального регистра суставов Англии, Уэльса и Северной Ирландии (NJR) и обнаружили, что металл‑металлические бедренные эндопротезы приходят в негодность заметно быстрее, например, керамических. Через пять лет после операции замене подлежали 6,2% первых эндопротезов и только 3,2% вторых.
В США некачественный протез может быть изъят из продажи самим производителем или FDA, однако за последние 20 лет регулятор всего три раза
воспользовался свои правом запретить поставки некачественного товара. В подавляющем большинстве случаев продажа эндопротезов приостанавливалась производителем, но это происходило, как правило, когда счет жалоб и судебных исков приближался к сотне или тысяче. Закон обязывает компании информировать FDA об отзыве продукции, если она может нанести вред здоровью. Согласно этим данным, с 2002‑го по 2013 год шесть лидирующих производителей отозвали из продажи 578 разновидностей бедренных эндопротезов и их составных частей.
Например, компании DePuy, ортопедическому подразделению фармгиганта Johnson&Johnson, понадобилось три года, чтобы снять с продажи эндопротез системы ASR. Причем еще в 2007 году инженеры DePuy провели тест на внутреннюю износостойкость системы и обнаружили, что по сравнению с другими эндопротезами при пользовании ASR в ткани бедра попадает очень много частичек металла. Несмотря на результаты тестов, DePuy продолжала продавать эти бедренные имплантаты. В 2009 году, получив около 400 жалоб от пациентов, FDA обратилось к DePuy c просьбой предоставить дополнительные данные об эндопротезах ASR, в том числе уточнения по их конструкции и результаты испытаний внутри компании. Кроме того, FDA сообщило Johnson&Johnson, что в крови пациентов, которым были установлены металл‑металлические протезы DePuy, была обнаружена высокая концентрация ионов металлов. По сведениям британского и австралийского национальных независимых регистров, эндопротезы ASR показали намного более низкую надежность, чем было заявлено производителем. По данным NJR, в течение пяти лет ревизионная (повторная) операция понадобилась 13% пациентов, которым была установлена система ASR XL для тотального эндопротезирования тазобедренного сустава, и 12% людей, которым установили систему ASR для поверхностного эндопротезирования (с сохранением головки бедренной кости).
Тем не менее решение окончательно отозвать ASR с рынка DePuy приняла только в августе 2010 года, спустя три года после получения первых данных о недостатках медизделия. К моменту прекращения продаж эндопротезы ASR были установлены 93 тысячам пациентов по всему миру, из которых около трети проживали в США. В ноябре 2013 года Johnson&Johnson сообщила, что выделит $4 млрд на удовлетворение исковых требований, связанных с дефектными суставами компании. К июню 2014 года в суд с исками обратились 12 тысяч человек.
Более 300 тысяч человек по всему миру (из них 200 тысяч в США) получили дефектные суставные эндопротезы компании Stryker – Rejuvenate и ABG II. Пациентам обещали, что устройства прослужат десятилетия, но у некоторых проблемы начались всего через два года. В июне 2012 года, получив официальное предупреждение от FDA, компания Stryker добровольно изъяла из продажи Rejuvenate и ABG II, сообщив хирургам, что изделия могут нанести вред тканям бедра и привести к более тяжелым последствиям. В ноябре 2014 года компания согласилась выплатить $1,43 млрд, чтобы удовлетворить претензии пациентов, которым были установлены неисправные бедренные эндопротезы. Соглашение Stryker включало в себя 3 тысячи судебных исков в штатах Миннесота и Нью‑Джерси. Каждый истец, перенесший ревизионную операцию, получил право на выплату от $300 тысяч.
Похожая история случилась с эндопротезом компании Zimmer. В 2006 году FDA одобрило их продукцию, бедренный компонент Дюрома, более известный как Durom Cup, и уже через год появились первые жалобы пациентов. В апреле 2008 года известный американский хирург‑ортопед и наемный консультант Zimmer Лоуренс Дорр сообщил компании, что Durom Cup вызывает у его пациентов мучительные боли. В ответ руководство Zimmer заявило, что с эндопротезом все в порядке, а в проблемах пациентов виноват сам Дорр, который неправильно его устанавливает. Под давлением FDA компания на несколько месяцев приостановила продажу устройства, объяснив это недоработками в руководстве по пользованию и установке эндопротезов. Издав новые инструкции для хирургов, Zimmer снова вернула Durom Cup на рынок, где устройство продержалось до конца 2010 года. В итоге к 2014 году компания Zimmer выплатила пострадавшим около $600 млн компенсации.
Причина проблем в том, что FDA начало регулировать продажу изделий медицинского назначения только в 1976 году. Законом были установлены разные требования к проведению испытаний различных медицинских изделий, в зависимости от потенциального риска или их роли в жизни и здоровье пациента. Когда закон вступил в силу, металл‑металлические эндопротезы уже успешно продавались на американском рынке, и FDA решило считать их изделиями со «средней степенью риска». Благодаря этому производители искусственных суставов могли получать одобрение регулятора по упрощенной схеме: компания должна была лишь продемонстрировать, что новый эндопротез – это версия уже продававшихся имплантатов. Проводить дорогостоящие клинические испытания, доказывающие эффективность и безопасность устройств, было необязательно.
37 лет FDA смотрело на рынок эндопротезов сквозь пальцы, и только после серии разразившихся в отрасли скандалов в январе 2013 года регулятор решился ужесточить требования и перевести металл‑металлические эндопротезы в разряд изделий с «высокой степенью риска». Сегодня производители могут получить одобрение FDA на продажу бедренных металлических эндопротезов только после проведения успешных клинических испытаний.
ортопедический рынок, эндопротезы, эндопротезирование, ортопедия, ортопедическое оборудование, ортопедическая клиника
Подписывайтесь на наш канал в Telegram Подписывайтесь на наш канал в Яндекс Дзен
Поделиться в соц.сетях
+1 +1 +1 +1