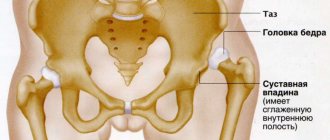
Межостистый неоартроз – это патология, при которой в различных отделах позвоночника образуется ещё один сустав, называемый ложным.
Такой дополнительный сустав развивается из-за излишнего сближения межостистых отростков, что нередко приводит к появлению новой суставной поверхности.
Обычно неоартрозу подвержены мужчины и женщины старше 60 лет, у которых наблюдаются и другие дегенеративно-дистрофические изменения позвоночника, например, остеохондроз. В молодом и среднем возрасте это заболевание возникает достаточно редко.
Медицинское описание
Любые деформационные явления в области позвонков становятся причиной разрастания костей, что уменьшает расстояние между ними и приводит к созданию волокнистых структур. В результате пациент страдает от сильного болевого синдрома, скованности и ограничения двигательных функций позвоночника.
Заболевание характеризуется формированием новых суставов, что объясняется сближением отростков позвонков. В официальной медицине патологию также называют межостистым неоартрозом.
Пациенты, которые перенесли серьезные травмы, с возрастом начинают ощущать сильную боль и ощущение дискомфорта. Связано это с обламыванием отростка позвонка и образованием ложной суставной ткани. При наличии проблем со щитовидной железой начинается формирование унковертебрального лжесустава. Что касается дополнительных факторов, которые способствуют прогрессированию патологии, то к ним относят:
- Всевозможные воспаления в области позвонков и хрящевых соединений.
- Возрастной фактор.
- Механические повреждения суставов.
- Дегенеративно-дистрофические процессы.
- Аномалии врожденного характера.
- Другие искривления.
При интенсивных возрастных изменениях не исключается травматизм хрящевых тканей, приводящий к отламыванию или изменению структуры позвонков. В результате патологии в пораженной области начнет образовываться неоартроз.
Последствия от таких изменений проявляются в виде снижения лабильности позвонка, стискивании спинного мозга, а также нарушения функциональности отдельных органов и систем.
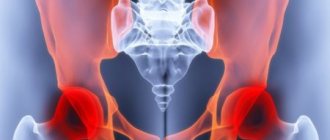
При прогрессировании заболевания и сопутствующих возрастных изменениях у пациентов могут начаться дегенеративные процессы в тазобедренных суставах. Зачастую это замечается у женщин. Из-за деструкции костной ткани на поврежденном месте развивается неоартроз.
Следует отметить, что неоартроз тазобедренного сустава практически не проявляется у детей и подростков. Случаи заболевания патологией в молодом возрасте крайне редки.
В современной медицине существует одна интересная практика, которая подразумевает искусственное наращивание ложного сустава при развитии отдельных патологических процессов в зоне бедра. Подобный подход может повлиять на образование новой суставной головки и впадины, позволяя избавиться от гнойно-воспалительных осложнений.
Основная симптоматика
Первым и ключевым признаком развития неоартроза является интенсивный болевой синдром в пораженной области. Зачастую боль проявляется после серьезных физических нагрузок, бега или длительного пребывания на ногах. Во время сна и отдыха она исчезает. На ранних стадиях болевые ощущения замечаются в течение короткого промежутка времени, но затем они усиливаются и становятся постоянными. В зависимости от локализации выделяют ряд других симптомов:
- Деформационные процессы в области шейного отдела, приводящие к мигреням, головокружению, нестабильному артериальному давлению и прочим неприятностям.
- Пульсирующие боли в области поясничного отдела при выполнении движений туловища. Синдром усиливается после продолжительного пребывания в положении сидя.
Если патология продолжает прогрессировать, а нужные меры не принимаются, пациент может пострадать от контрактуры опорного сустава, таза, бедер и коленей.
Любые осложнения негативно сказываются на трудоспособности пациента, в результате чего нижние конечности становятся практически неподвижными. Постоянная боль вызывает ощущение скованности, а также повышает риск развития остеохондроза, полиартрита и прочих более опасных заболеваний.
В большинстве случаев неоартрозы поясничного отдела связаны с естественными возрастными изменениями, однако бывают и другие причины. Очень часто патология проявляется после:
- Воспалений в хрящевых тканях позвонков и дисков.
- Дегенеративных изменений из-за перенесенных травм.
Унковертебральный неоартроз шейного отдела позвоночника
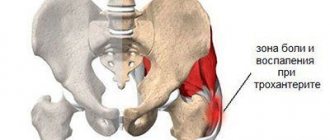
Унковертебральный неоартроз часто поражает шейный отдел позвоночного столба. Это заболевание характеризуется тем, что на задних поверхностях тел позвонков формируются патологические выступы. Это отложение солей кальция. Они соприкасаться с соседними телами позвонков и провоцируют их разрушение за счет трения костной ткани. В результате на противоположной стороне также формируются ложные костные отростки. В итоге они соединяются между собой с помощью плотной фиброзной ткани. Позвоночник утрачивает привычную подвижность. Любые движения головой начинают причинять боль.
Унковертебральный неоартроз шейного отдела провоцируется следующие клинические симптомы:
- частые головные боли, локализующиеся в затылочной части;
- головокружение, слабость, сонливость, снижение умственной работоспособности, чувство хронической усталости;
- хруст в области шеи при попытке совершать круговые движения головой;
- повышение артериального давления без видимой для этого причины.
Неоартроз шейного отдела формируется в возрасте 30 – 40 лет. Поначалу он не доставляет особых проблем. Но по мере уплотнения фиброзной капсулы ложного сустава симптомы нарастают. Появляется постоянная ноющая боль в области задней поверхности шеи. Возникает ощущение стянутости, чрезмерного напряжения мышц в области шеи и воротниковой зоны.
Неоартроз шейного отдела позвоночника поражает позвонки С3 – С6, поэтому быстро возникает нарушение иннервации щитовидной железы, тканей горла и плечевого нервного сплетения. У пациентов возникает ощущение сложности при проглатывании твердой пищи. Появляются парестезии в верхних конечностях, чувство онемения мизинцев и больших пальцев рук.
Если унковертебральный неоартроз шейного отдела позвоночника не лечить своевременно, то постепенно остеофиты полностью ограничат подвижность и начнется вторичное дегенеративное разрушение хрящевых и костных тканей. Для лечения лучше всего обращаться к вертебрологу. Участковый терапевт в городской поликлинике вряд ли сможет назначить эффективное и безопасное лечение. Как правило, пациентам с подобными деформациями устанавливается не совсем верный диагноз – остеохондроз. Соответственно, назначается лечение, которое не может дать положительного результата.
Эффективная диагностика
Что касается диагностирования неоартроза, то оно подразумевает составление общей картины после сбора врачом-неврологом анамнеза. Специалисту важно оценить время появления патологии, специфику болевого синдрома, а также список симптомов, которые возникли после развития проблемы.
Также во время диагностики необходимо проводить полноценный медицинский осмотр, обращая внимание на появление болей в голове при изменении положения тела, скачки артериального давления и прочие сопутствующие симптомы. Чтобы повысить точность диагностирования, следует применить:
- Рентгеновское обследование и компьютерную томографию.
- КТ-миелографию, которая заключается в применении контрастного вещества для определения врожденных аномалий или вероятности повреждений позвонков.
- Магниторезонансую терапию. Эта методика считается наиболее эффективной, поскольку она указывает не только на состояние костной ткани, но и на изменения в области мягких тканевых соединений.
- Рентгеновское обследование и компьютерную томографию.
- КТ-миелографию, которая заключается в применении контрастного вещества для определения врожденных аномалий или вероятности повреждений позвонков.
- Магниторезонансую терапию. Эта методика считается наиболее эффективной, поскольку она указывает не только на состояние костной ткани, но и на изменения в области мягких тканевых соединений.
Тип и форма диагностики определяются специалистом после получения анамнеза, учета индивидуальных жалоб больного, а также других данных.
Также следует провести дифференциальное диагностирование, чтобы исключить ишиас, люмбалгию, онкологические заболевания и любые другие формы артроза.
Причины межостистого неоартроза
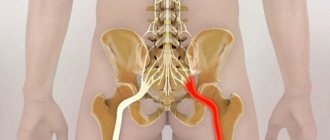
Межостистый неоартроз – это самый распространённый вид патологии. Он локализуется в шейном и поясничном отделах позвоночного столба. Здесь в норме присутствует естественный прогиб позвоночника кпереди. За счет лордоза происходит максимальное сближение остистых отростков, которые в ряде случаев могут соприкасаться друг с другом.
Причины развития неоартроза в этих и других отделах позвоночного столба следующие:
- нарушение осанки и искривление позвоночного столба в виде усиления лордоза на фоне увеличенного грудного кифоза (круглая спина, сутулость);
- снижение высоты межпозвоночных дисков (протрузия) на фоне длительного течения дегенеративного дистрофического заболевания (дорсопатия);
- спондилоартроз и спондилолистез – провоцируют появление трещин на остистых и поперечных отростках позвонков, что может стать причиной формирования ложного сустава;
- болезнь Бехтерева или анкилозирующий спондилит – провоцирует формирование рубцовой ткани между телами позвонков, образует ложные суставы и прочные спайки остистых отростков, препятствует подвижности позвоночного столба;
- ревматоидные процессы, системная красная волчанка;
- заболевания эндокринной системы, например, неоартроз шейного отдела позвоночника в большинстве случаев провоцирует заболевание щитовидной железы;
- избыточная масса тела;
- ведение малоподвижного образа жизни без достаточной физической нагрузки на спину;
- неправильная постановка стопы с неравномерным распределением амортизационной нагрузки;
- травмы спины и воротниковой зоны (удары, растяжения связочной и сухожильной ткани, переломы тел позвонков и их остистых отростков, трещины костной ткани);
- инфекции спинного мозга и тканей позвоночного столба (остеомиелит, туберкулез, полиомиелит и т.д.).
Исключить все вероятные причины развития данной патологии очень сложно. Нужно следить за своим весом и осанкой, правильно организовать спальное и рабочее месте, своевременно обращаться к вертебрологу при появлении любых болей в области позвоночного столба.
Способы лечения и профилактические меры
Что касается способов лечения неоартроза, то они бывают как консервативными, так и хирургическими. В первом случае лечебные действия направлены на борьбу с причинами, вызвавшими дегенеративные процессы в области костной ткани. Также консервативные методики улучшают циркуляцию крови и питание суставов ценными веществами, снижают интенсивность болевого синдрома. При развитии сильных болей пациенту назначают постельный режим и полный отказ от физической активности.
Существуют и другие методы, которые относятся к вспомогательным профилактическим мерам. Речь идет о бальнеотерапии, гирудотерапии и посещении бассейна. Это помогает снизить нагрузку на позвоночник. Регулярные занятия лечебной физкультурой способствуют укреплению мышечного корсета, восстанавливают естественный обмен веществ в суставных тканях, а также стабилизируют подвижные функции позвонков.
Если заболевание переходит в острую стадию, консервативные методы лечения могут оказаться бесполезными. В таком случае приходится задействовать оперативное вмешательство, выполняя операции по удалению остеофитов (разросшихся отростков позвонков).
При выполнении операции пациенту может дополнительно понадобиться восстановление позвоночного диска методом протезирования. В результате хирургических действий нормальное движение суставов восстанавливается, а болевой синдром полностью исчезает.
Лечение неоартроза позвоночника
Начинать лечение неоартроза необходимо с проведения тщательной диагностики. Назначается рентгенографический снимок в разных проекциях, КТ-миелография и МРТ обследование. После уточнения диагноза принимается решение о проведении консервативного лечения неоартроза позвоночника или необходимости хирургического вмешательства.
При первой и второй степенях развития ложного сустава предлагается консервативная терапия. В нашей клинике мануальной терапии курс восстановительного лечения может включать в себя:
- тракционное вытяжение позвоночного столба, которое позволяет восстановить физиологическое положение тел позвонков, расправить междупозвоночные диски и устранить компрессионное давление на корешковые нервы;
- остеопатия и массаж для восстановления эластичности тканей, усиления микроциркуляции крови и лимфатической жидкости;
- лечебная гимнастика и кинезиотерапия – для купирования процессов формирования фиброзной капсулы и увеличения амплитуды подвижности позвоночника;
- рефлексотерапия, физиотерапия, лазерное воздействие и многое другое.
Лечение унковертебрального неоартроза шейного отдела позвоночника также включает в себя массаж воротниковой зоны и специальный курс лечебной гимнастики, который направлен на восстановлении подвижности и увеличения амплитуды совершаемых головой движений.
Если вам требуется лечение неоартроза позвоночника, то рекомендуем вам записаться на бесплатный прием к вертебрологу в нашей клинике мануальной терапии. Здесь вы получите исчерпывающую информацию по вашему случаю заболевания от лечащего врача.
Патологии височно-нижнечелюстного сустава
Еще одной распространенной формой патологии является неоартроз ВНЧС. Он подразумевает формирование ложных суставов в области нижней челюсти. В таком случае суставная головка начинает менять свое естественное положение, способствуя развитию нового отростка. В большинстве случаев проблему вызывают всевозможные воспаления и перенесенные травмы.
Специалисты выделяют три стадии неоартроза ВНЧС, которые отличаются симптоматикой и формой протекания. На первой стадии патология называется остеоартритом и может длиться до полугода. В пораженной области замечается сильное воспаление, которое приводит к гибели костной ткани. Наиболее уязвимым местом становится суставной хрящ, который серьезно деформируется.
К сожалению, провести эффективную диагностику и определить такое заболевание бывает проблематично, а иногда и невозможно, ведь существенных дегенеративных изменений в ткани костей практически нет. Только при тщательном обследовании на высокотехнологичном рентгеновском оборудовании можно заметить деформацию тканей.
Проблема неоартроза ВНЧС возникает у детей и подростков. При отсутствии эффективного лечения патология переходит с первой стадии во вторую. В таком случае начинается полная гибель головки нижней челюсти, а проведение рентгена уже определяет ряд изменений в хрящевой ткани. Вторая стадия может занимать от одного года до трех лет, при этом у некоторых маленьких пациентов патология останавливается в такой форме и не прогрессирует. Что касается подвижности нижней челюсти, то она становится очень слабой.
Существует и третья стадия неоартроза ВНЧС. Ее называют выраженной репарацией. Развитие такой патологии приводит к существенной деформации височной кости, что можно заметить при рентгеновском обследовании. Также суставный бугорок начинает сглаживаться, становясь похожим на прямую линию. Продолжительность третьей стадии достигает семи лет, а подвижные функции сустава практически теряются.
Последняя стадия, четвертая, приводит к окончательной скованности челюсти. Зачастую ее замечают у пациентов в подростковом возрасте.
Развитие псевдоартроза
При перенесении серьезных травм или дегенеративных изменений у пациента может начать развиваться псевдоартроз бедренной кости. Как известно, полноценное восстановление тканей при переломах может занимать около 4—6 месяцев (точный срок определяется сложностью патологии). В течение этого промежутка времени суставы начинают сращиваться, что удается определить с помощью рентгена.
Однако иногда этого временного промежутка не хватает из-за замедленной консолидации. В таком случае после заживления суставов линия перелома становится практически гладкой и незаметной. Однако по истечении определенного времени она расширяется, а в образованном промежутке появляется костная ирритационная мозоль без выраженных контуров. Ее называют псевдоартрозом.
Специалисты выделяют несколько разновидностей репаративной регенерации костной ткани. На ранних стадиях развития патологию называют первичной. В таком случае замечается сращивание костных соединений с помощью остеогенеза. Такое явление вызывает образование интермедиарной мозоли.
При сращивании костей без щелей начинается первично-замедленная стадия, которая указывает на частичную регенерацию костной ткани. Вторичное сращивание приводит к формированию разных видов мозолей, а также увеличению срока заживления.
Предрасполагающие факторы
Предрасполагающие факторы
Причины развития псевдоартроза бывают самыми различными. Выше упоминалось, что неоартроз может быть врожденным или приобретенным. В случае с этой патологией ситуация обстоит аналогично. Однако врожденные заболевания замечаются в редких случаях и могут проявляться при внутриутробных изменениях или сбоях в формировании костей. Также этому способствуют расстройства генетического характера.
Что касается второго фактора, то он проявляется при таких провокаторах:
- Перенесении многочисленных изменений и дегенеративных процессов.
- Смещении фрагментов костей.
- Нарушении остеосинтеза.
- Присоединении вторичной инфекции.
- Нарушенной циркуляции крови.
Также проблему нередко вызывают различные патологии, способствующие ухудшению обменных процессов. Этот фактор проявляется у людей, страдающих избыточным весом.
Есть и инфекционные провокаторы, нарушения в кровообращении и множественные травмы. При комбинированных поражениях вероятность развития псевдоартроза становится максимально высокой.
Клиническая картина
Чтобы диагностировать псевдоартроз в крестцовом или поперечном отделе, необходимо иметь представление о клинической картине. Первые признаки патологии заключаются в следующем:
- Появление подвижности в тех областях, где она отсутствовала. Также у пациента может замечаться изменение амплитуды или направления движений. Как известно, у здоровых людей эти явления полностью исключены, а у пациентов с псевдоартрозом замечалась способность поворачивания руки или ноги на 360 градусов.
- Укорочение конечности. Является наиболее серьезным признаком дегенеративных изменений. В таком случае разница между обеими конечностями может достигнуть 10 сантиметров.
- Изменения в области мышц, снижение силы.
- Лишение конечностей естественной функциональности, которое проявляется при выполнении базовых упражнений или минимальных нагрузок. При развитии нарушений пациент не может опираться на ногу, совершать прыжки и даже ходить.
- Нарушения в работе истинных суставов из-за недостающей нагрузки.
Зная, как диагностировать патологию, необходимо приступать к соответствующим способам лечения. Чем быстрее будут приняты правильные меры, тем эффективнее будут лечебные мероприятия и срок сращивания поврежденных костных тканей.
Рост оперативной активности травматологов-ортопедов в последние 15-20 лет. Увлечение молодых врачей освоением новых методик хирургического лечения пациентов с переломами шейки бедра и костей таза с использованием погружных металлофиксаторов, в ущерб использованию ранее хорошо зарекомендовавшим себя консервативным методам и методам аппаратного лечения переломов. Расширение показаний к эндопротезированию тазобедренного сустава и внедрение этого высокотехнологичного метода, обеспечивающего при правильном его применении отличные результаты, в повседневную практику хирургов обычных травматологических отделений по всей стране привело к увеличению числа больных, страдающих послеоперационным остеомиелитом костей составляющих тазобедренный сустав. Не уменьшается и количество пациентов страдающих посттравматическим, огнестрельным и гематогенным остеомиелитом проксимального отдела бедра и вертлужной впадины.
Лечение пациентов с данной тяжелой патологией крайне трудоемко, длительно и дорогостояще, нередко сопряжено с потерей пациентом трудоспособности, а в некоторых случаях заканчивается летальным исходом.
По данным Hanssen et al. (1996), стоимость лечения пациента без учета заработной платы врачей и среднего медицинского персонала, с гнойно-воспалительным процессом, развившимся в ранние сроки после операции эндопротезирования тазобедренного сустава, составляет 80000 долларов США, а пациента с поздним инфекционным осложнением — до 140000 долларов (7).
Таким образом, проблема хирургического купирования гнойно-воспалительного процесса, развившегося в области тазобедренного сустава с восстановлением опорной функции конечности, по сей день остается чрезвычайно сложной и актуальной (8)
Впервые хирургический метод лечения больных с гнойно-воспалительными процессами в области тазобедренного сустава был применен в Х1Х веке. В 1821г. резекционную артропластику тазобедренного сустава больному септическим артритом выполнил Antoni White. В результате операции сформировался неоартроз, который, в связи со смертью больного от чахотки, был морфологически изучен через 5 лет. После введения в хирургическую практику антисептического метода, острого долота вместо ножовки, появления рентгенографического метода резекционная артропластика тазобедренного сустава завоевала право операции выбора при огнестрельных ранениях, туберкулезных и неспецифических кокситах (15).
Внедрение в 20-х годах ХХ века гемотрансфузии, в 30-х годах — сульфаниламидных препаратов и особенно антибиотиков в конце 40-х годов, а также совершенствование методов асептики и антисептики обусловило переход операции из казуистической в разряд регулярно применяющихся вмешательств.
В 20 — 30-х годах ХХ века резекция проксимального отдела бедра с введением его в вертлужную впадину получила известность как операции Lexer-Whitmann. Метод предполагал под собой отсечение большого вертела в косом направлении с прикрепляющимися к нему мышцами. После вскрытия полости сустава осуществлялась резекция шейки бедра с удалением ее головки. Остаток шейки бедренной кости закруглялся и покрывался лоскутом жира, после чего вправлялся в вертлужную впадину. Ранее отбитый участок большого вертела крепился ниже своего основания на освеженный участок бедра с помощью шурупов. Конечность фиксировалась в тазобедренной гипсовой повязке (21, 22).
В 1924 году W.Ansch?tz сделал сообщение о 22 реконструктивных операциях, выполненных им при различных заболеваниях тазобедренного сустава (паралитические болтающиеся суставы, застарелые врожденные вывихи, болезнь Пертеса, инфекционные артриты, деформирующие артрозы, несросшиеся переломы и псевдоартрозы шейки бедра) (16).
В 1928 году GR.Girdlestone разработал и внедрил свой вариант резекционной артропластики тазобедренного сустава для лечения больных с септическим артритом и кокситом туберкулезной этиологии (20).
Суть операции состояла в создании параллельных площадок с наибольшей поверхностью соприкосновения между резецированным в косом направлении по межвертельной линии бедренной костью и частично резецированной в верхних и задних отделах вертлужной впадиной. Между этими компонентами укладываются лоскуты из рубцовой или мышечной ткани с целью создания условий для формирования неоартроза. Конечность фиксировалась в тазобедренной гипсовой повязке в течение 1 месяца.
В 1939 году P.C.Colonna опубликовал сообщение о том, что в Америке предложенная им операция была произведена 121 пациенту. Процент отличных и хороших результатов колебался в пределах 70-85% (19).
Основными моментами операции автор считал сохранение фиброзно-мышечного слоя на вершине большого вертела и пересадку абдукторов как можно ниже на диафиз бедра. В вертлужную впадину автор внедрял не культю шейки бедра, а большой вертел. Операция получила сначала название как операция Ansch?tz-Colonna, а позже как операция Colonna 2.
Обе операции, как Lexer-Whitmann, так и Ansch?tz-Colonna предполагали длительную фиксацию резецированного конца бедра, внедренного в вертлужную впадину в тазобедренной гипсовой повязке в положении отведения конечности под углом в 40-45 градусов. Через 3-5 месяцев производилась корригирующая остеотомия бедра для устранения этого порочного положения.
Впервые в истории медицины результаты лечения повреждений тазобедренного сустава на большом материале были изучены во время и после окончания Великой Отечественной войны. Так, М.О.Фридланд (1944) закруглял шейку при резекции бедра. То же самое в 1947 году рекомендовал и осуществил 4 раза с отличным функциональным результатом Б.П.Кириллов (2, 14).
Оригинальную методику обработки шейки при резекции тазобедренного сустава по поводу огнестрельных ранений предложил А.А.Полянцев (1944). Он проводил линию распила шейки под углом, сверху вниз и кнаружи (10).
В годы войны М.П.Скрынченко прооперировал 36 раненных солдат и офицеров с огнестрельными повреждениями тазобедренного сустава. Перед внедрением большого вертела в вертлужную впадину он придавал большому вертелу форму конуса. У 31 пациента был получен подвижный опорный сустав, 5 пациентов умерло (13).
В 40-х годах ХХ века появилась идея о замещении суставного конца бедра металлическим протезом. H.K.Bohlman (1939) впервые применил виталлиевый протез на ножке в виде 3-х лопастного гвоздя со сферической головкой (17). В 1952 году Moor применил металлический эндопротез с перфорированной ножкой.
В 50-60-х годах ХХ века J.Charnley разработал и внедрил в хирургическую практику эндопротез собственной конструкции с чашкой из высокомолекулярного полиэтилена для тотального эндопротезирования тазобедренного сустава с использованием костного цемента (18).
Основы тотального эндопротезирования тазобедренного сустава в нашей стране были заложены К.М.Сивашом, выступившим с докладом по данному вопросу в 1956 году.
На первом этапе освоения метода эндопротез Сиваша предназначался для лечения больных анкилозирующим спондилоартритом (болезнь Штрюмпелля-Бехтерева-Мари). Метод лечения оправдал возлагавшиеся на него надежды. Положительный опыт лечения больных привел к расширению диапазона заболеваний, при которых стали применять эндопротез Сиваша — ревматоидный артрит, деформирующий коксартроз (11).
Вместе с тем, у зарождающегося нового метода лечения больных с патологией тазобедренного сустава были и свои оппоненты. Так, Е.Т.Скляренко (1974) высказывал мнение о том, что «биологическую артропластику нельзя заменить искусственными суставами. Проблема их применения еще далека от разрешения. Искусственные тазобедренные суставы допустимы лишь в тех случаях, когда биологическая артропластика по каким-либо причинам не может быть выполнена, в основном у людей пожилого возраста» (12).
С критикой метода выступал Г. Кайзер (1974), который в своей работе о. У молодых людей автор предлагал выполнять по показаниям артродез тазобедренного сустава, у пожилых больных — резецировать головку и всю шейку бедра с созданием неоартроза (3).
С внедрением в широкую практику метода эндопротезирования тазобедренного сустава появилась проблема лечения гнойных осложнений.
В 1974 году К.М.Сиваш и В.Н.Гурьев на основе анализа результатов лечения 830 больных, оперированных в 1959-1973гг. в ЦИТО обозначили абсолютные противопоказания к операции эндопротезирования тазобедренного сустава: нагноительные процессы в области сустава; наличие свищей и послесвищевых рубцов; наличие свежих элементов активной туберкулезной гранулемы; наличие очага инфекции в организме больного; рубцовые изменения тканей в области тазобедренного сустава в результате ранее перенесенных операций; коксартроз, развившийся в результате перенесенного пациентом гнойного коксита; отсутствие специальной операционной, в которой проводятся только «чистые» операции, и специального отделения, в котором находятся больные после тотального эндопротезирования тазобедренного сустава (11, 1).
А.А.Покрывалов (1987) на основании проведенного статистического анализа результатов 766 эндопротезирований тазобедренного сустава, выполненных в ЦИТО с 1975 по 1983 гг. доказал, что «наиболее существенным фактором, предрасполагающим к возникновению гнойных осложнений после эндопротезирования, является наличие предшествующей эндопротезированию операции на данном суставе» (9).
Мы в ходе анализа сроков развития гнойно-воспалительного процесса у 115 эндопротезированных больных, лечившихся в ЦИТО с 1975 по 2002 гг, обнаружили следующую закономерность (5).
Из 13 больных, которым эндопротезирование было выполнено при наличии анамнестических данных о ранее перенесенном гнойно-воспалительными процессе в области заинтересованного сустава, либо сепсисе, нагноительный процесс в течение 1 года развился у 11 больных (84,6%), а в поздние сроки — у 2-х (15,4%). Средний срок развития нагноения оказался равным 5 месяцам.
Из 36 больных, которым производились те или иные операции на заинтересованном суставе, нагноительный процесс в течение 1 года развился у 24 пациентов (66,7%), в поздние сроки — у 12 больных (33,3%). Средний срок развития нагноения 1 год.
Из 66 больных, которым эндопротезирование было выполнено на интактном суставе, в течение 1 года нагноение развилось у 34 пациентов (51,5%), в поздние сроки у 32 больных (48,5%). Средний срок развития гнойно-воспалительного процесса оказался равным 2 годам 8 месяцам.
То есть, наибольший риск, в плане развития гнойных осложнений, был связан с эндопротезированием тазобедренного сустава больным, в анамнезе которых отмечался тот или иной гнойно-воспалительный процесс или у которых имелись послеоперационные рубцы в области сустава.
Другими словами, проведенный анализ подтвердил известный тезис классиков метода о необходимости дифференцированного подхода к отбору пациентов, которым показано выполнение эндопротезирования тазобедренного сустава с благоприятным отдаленным результатом.
В настоящее время помимо специализированных центров по эндопротезированию крупных суставов с обученным персоналом, высококвалифицированными хирургами, соблюдающими строгий отбор больных, оперирующими в операционных с ламинарным потоком воздуха с минимальной кровопотерей и в кратчайший временной промежуток, метод стал широко внедряться в практику работы травматологических отделений обычных городских больниц по всей стране.
По данным разных авторов, ежегодно в мире выполняется от 1 до 1,5 миллионов тотальных замещений тазобедренного сустава. В России в начале 90-х выполнялось 3200 подобных операций в год, в то время как ориентировочная ежегодная минимальная потребность в эндопротезах по РФ составляет 20-25 тысяч, а максимальная 100 тысяч (4).
Многие хирурги при принятии решения о необходимости эндопротезирования тазобедренного сустава все чаще игнорируют наличие хронического гнойно-воспалительного процесса в области тазобедренного сустава у пациента или латентного очага инфекции в организме, не говоря уже о наличии рубцово-измененных тканей после ранее перенесенных реконструктивных операций на тазобедренном суставе. По данным разных авторов, процент гнойных осложнений после эндопротезирования колеблется в пределах от 0,2 до 58,5%. (5).
Основными методами лечения гнойно-воспалительных процессов в области тазобедренного сустава в настоящее время является одно или двухэтапное эндопротезирование сустава либо его артродезирование с использованием различных металлофиксаторов или тазобедренной гипсовой повязки (8, 6).
Соглашаясь с мнением родоначальников метода эндопротезирования о нецелесообразности его использования в лечении больных с гнойно-воспалительными процессами и опираясь на наш многолетний опыт лечения больных с этой тяжелой патологией, считаем что проведение эндопротезирования тазобедренного сустава больным с гнойно-воспалительными процессом крайне опасно из-за высокого риска развития как ранних, так и поздних послеоперационных гнойных осложнений.
Проведение операций по артродезированию тазобедренного сустава больным с гнойно-воспалительным процессом с использованием как погружных, так и внешних фиксаторов, включая тазобедренную гипсовую повязку, мы считаем также неправильным. С нашей точки зрения, артродезирование сустава при данной патологии чревато развитием нагноительного процесса в области фиксатора с возникновением необходимости его раннего удаления и остающейся нерешенной проблемой купирования гнойно-воспалительного процесса, но в худших условиях, чем до выполнения артродеза, во-первых. Во-вторых, в случае достижения анкилоза очень высок риск развития рецидивов остеомиелитического процесса с появлением необходимости проведения в последующем многократных фистулсеквестрнекрэктомий. В-третьих, даже при отсутствии инфицирования и дестабилизации тех или иных фиксаторов высоким остается риск развития несостоятельности артродеза на фоне некупированного гнойно-воспалительного процесса с необходимостью выполнения повторных оперативных вмешательств.
Адекватной альтернативой, как эндопротезированию, так и артродезированию тазобедренного сустава при гнойно-воспалительных процессах, по нашему мнению, является выполнение резекционной фистулсеквестрнекркэтомии проксимального отдела бедра и вертлужной впадины с созданием опорного неоартроза, что позволяет, как купировать нагноительный процесс, так и добиться хорошего функционального результата для больного.
С 1985 по 2005 год нами на базе отделения «гнойных осложнений и последствий травм опорно-двигательной системы» ЦИТО и отделения «гнойной хирургии» ЦВГ при «Спецстрое России» прооперировано 75 больных с гнойно-воспалительными процессами в области тазобедренного сустава (хронический и острый послеоперационный, посттравматический, гематогенный, огнестрельный остеомиелиты) в возрасте от 9 до 75 лет. У всех больных удалось купировать нагноительный процесс и добиться формирования опорного неоартроза с восстановлением опорной функции конечности практически в полном объеме.
С целью улучшения результатов лечения больных с данной патологией нами разработан и внедрен комплекс лечебно-реабилитационных мероприятий направленный на купирование нагноительного процесса с формированием опорного неоартроза в суставе и восстановлением опорной функции конечности.
Комплекс лечебно-реабилитационных мероприятий, направленный на купирование гнойно-воспалительного процесса.
- Радикальная санация местного патологического очага путем удаления всех некротизированных тканей, иссечение свищевых ходов на всем протяжении, секвестрнекрэктомия остеомиелитически измененных участков костной ткани.
- Налаживание адекватного ирригационно-вакуумного дренирования послеоперационной раны с длительным ее промыванием растворами антисептиков.
- Адекватная антибактериальная терапия: начало проведения антибактериальной терапии за 2 часа до операции препаратами широкого спектра действия с последующей их корректировкой на 1 -2 день после операции на основании данных посева операционного материала, полученных как в аэробных, так и анаэробных условиях, а затем на основании данных посевов отделяемого из дренажей.
- Коррекция гомеостаза, иммунокоррекция.
- Программа функционального лечения больных с целью создания опорного неоартроза, которая состоит из 3-х этапов (приводится ниже).
- Профилактика рецидива.
Операция производится в положении больного на здоровом боку из наружне-бокового доступа. Следует отметить, что при наличии функционирующего свища необходимо выполнять тугое заполнение свищевого хода 2% спиртовым раствором бриллиантового зеленого, после чего производится разрез с иссечением послеоперационного рубца и свищевого хода на всем его протяжении. При наличии инфицированных металлоконструкций производится их удаление, а затем выполняется резекционная секвестрнекрэктомия проксимального конца бедренной кости и вертлужной впадины с иссечением всех окрашенных бриллиантовым зеленым и вызывающих сомнение в плане жизнеспособности тканей. При бессвищевой форме остеомиелита выполняется резекционная секвестрнекрэктомия проксимального отдела бедра и вертлужной впадины в пределах здоровой (кровоточащей) костной ткани. С помощью рашпиля и электрической дрели зачищается резецированный участок бедренной кости и удаляются все острые костные выступы и на вершине санированного проксимального конца бедренной кости в сагиттальном направлении выпиливается овальная неглубокая выемка.
Выемка обеспечивает более стабильный контакт бедренной кости и вертлужной впадины. Затем раневая полость обильно промывается растворами перекиси водорода и хлоргекседина, после чего тщательно вакуумируется с помощью отсоса. Больной переводится в горизонтальное положение, оперируемая конечность отводится до угла в 40-45 градусов и укладывается на дополнительный стерильный операционный стол с фиксацией стопы в нейтральной позиции в деротационном сапожке. Рана дренируется двумя дренажами. Однополюсной дренаж подводится к вертлужной впадине, а 2-х полюсной проводится в продольном направлении по длине всей раны под мышцами, после чего рана послойно плотно ушивается наглухо. После завершения операции больной переводится в палату без изменения заданного угла отведения со стопой фиксированной в деротационном сапожке. Такая фиксация, наряду с активным функциональным лечением в послеоперационном периоде, обеспечивает управляемый процесс формирования опорного неоартроза. С первого дня после операции начинается проведение комплексной программы реабилитации. За счет тяги околосуставных мышц проксимальный конец бедренной кости постепенно приближается к крыше вертлужной впадины. Эти костные структуры начинают контактировать и артикулировать, сформированная во время операции выемка создает условия для большей стабильности, одновременно формируются рубцы, которые удерживают проксимальный конец бедра у крыши вертлужной впадины. Временной промежуток с необходимостью постельного режима в среднем составляет 3-4 недели и напрямую связан с формированием рубцовой ткани в области формирующегося неоартроза. Основным показателем формирования достаточно крепкой рубцовой ткани является свободное удержание больным освобожденной из деротационного сапожка стопы в функционально правильной нейтральной позиции в течение суток. На этом этапе больной начинает обучаться сидению в постели и стоянию в палате на костылях с отведенной под угол в 20 градусов ногой с использованием обуви с набойкой на подошве для компенсирования анатомически функционального укорочения.
Программа функционального лечения больных с целью создания опорного неоартроза.
- А.
Ранний послеоперационный период (постельный режим до 30 дня после операции). 1-А. Ранний послеоперационный период — до 10 дня после операции. 2-А. Ранний послеоперационный период — с 10 по 20 день после операции. 3-А. Ранний послеоперационный период — с 20 по 30 день после операции. - Б.
Поздний послеоперационный период (с 30 дня и до выписки больного из стационара). - В.
Период реабилитации в амбулаторных условиях (до 6-8 месяцев после выписки больного из стационара).
Суть этих реабилитационных мероприятий состоит в том, что лечебная гимнастика для мышц оперированной конечности и туловища начинается с раннего послеоперационного периода в постельном положении с минимального числа упражнений и проводится в возрастающем темпе с течением времени.
Ранний послеоперационный период 1-А — до 10 дня после операции:
в горизонтальном положении отведения конечности под 45 градусов, со стопой фиксированной в нейтральном положении деротационной шиной до 5-10 минут 3 раза в день проводятся: изометрические упражнения для мышц оперированной и здоровой нижней конечности; щадящие пассивно активные сгибания в коленном суставе; присаживание в постели с использованием Балканской рамы; занятия для укрепления мышц рук и здоровой ноги с использованием резинового бинта или эспандера. На 5-7 день добавляются упражнения по активной попытке отрыва выпрямленной ноги от плоскости постели.
Ранний послеоперационный период 2-А — с 10 по 20 день после операции: на фоне продолжающихся упражнений, больной обучается свободному сидению в постели со спущенной здоровой ногой, и продолжительность занятий увеличивается до 10-15 минут 3 раза в день. В комплекс добавляются упражнения по разгибанию туловища с отрывом таза от плоскости постели до 50-100 раз в сутки.
Ранний послеоперационный период 3-А — с 20 по 30 день после операции:
продолжительность проведения занятий гимнастикой увеличивается до 15-20 минут 3 раза в день. Добавляют упражнения по активному сгибанию ноги в коленном суставе с попытками отрывать разогнутую оперированную ногу от постели до 100 раз в день. К 25 дню на некоторое время стопа вынимается из деротационного сапожка и фиксируется между валиками с песком.
Б. Поздний послеоперационный период — с 30 дня до выписки больного из стационара:
продолжительность занятий увеличивается до 20-30 минут 3 раза в день. Активные сгибания ноги в коленном суставе с попытками ее отрыва от постели увеличивают до 200 раз в день. Больного обучают стоянию и ходьбе на костылях с отведенной конечностью под угол в 20-30 градусов в обуви с набойкой для компенсации укорочения до 5 минут 3 раза в день. Добавляют упражнения по сгибанию и отведения ноги из положения стоя и самостоятельному присаживанию на стул с регулируемой высотой сидения (подкладываются подушки) до 10-15 упражнений 3 раза в день.
В. Период реабилитации больного в амбулаторных условиях:
на фоне продолжающегося реабилитационного комплекса из положения лежа и стоя до 45 минут 3 раза в день количество всех упражнений увеличивают до 100 в день. Больной ходит на отведенной конечности до 30 минут в день с нагрузкой на ногу до 10-15% от нормы с ежемесячным увеличением нагрузки еще на 10-15% а продолжительности ходьбы на 30 минут. С момента (в среднем 3-4 месяца после операции), когда пациент может свободно оторвать ногу от плоскости постели и удержать ее в таком положении некоторое время нога может быть приведена в функционально правильное положение с соответствующим уменьшением высоты набойки для компенсации анатомического укорочения. Больной постепенно переходит на ходьбу с одним костылем или тростью. В тот день, когда пациент встанет и забудет о необходимости взять в руки костыль или трость (в среднем 4-6 месяцев) он сможет постепенно переходить на ходьбу без дополнительной опоры.
ВЫВОДЫ:
Разработанный и внедренный нами метод по формированию опорного неоартроза качественно отличается от методов резекционной артропластики Lexer-Whitmann, Anschutz-Colonna и GR.Girdlestone, так как, во-первых, позволяет добиться купирования остеомиелитического процесса у больных, как правило, с запущенными, тяжело протекающими формами остеомиелита. Во-вторых, не требует длительной дополнительной фиксации оперированной конечности в тазобедренной гипсовой повязке, а напротив подразумевает под собой проведение активной реабилитационной программы, направленной на восстановление функции сустава. В-третьих, для формирования опорного неоартроза не требуется использования пластических материалов (жировой, мышечной и других видов ткани), так как в ходе лечения резецированные костные фрагменты закрываются собственной соединительной тканью. В-четвертых, при удачном исходе лечения по предложенному нами методу больной избавляется от воспалительного процесса, от болей в суставе, практически полностью восстанавливает опорную и двигательную функцию сустава и полностью избавляется от необходимости повторных оперативных вмешательств.