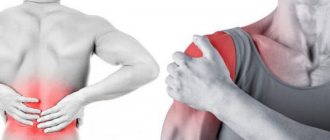
Мышечное переутомление
В наш технологичный век у многих постепенно формируется новая «вредная привычка». Проводя большую часть дня перед экраном компьютера или держа в руке мобильные гаджеты, мы можем даже не заметить, что сидим в совершенно неудобной и неестественной позе. Особенно «достается» мышцам плечевого пояса, шеи, спины и правой руки, которая постоянно находится на компьютерной мышке у офисных работников1. Длительное пребывание в одной позе или стереотипность движений могут привести к перенапряжению задействованных в работе мышц, которое мы ощущаем как болезненность1.
Физическая нагрузка
«Ломота» в теле после физической нагрузки может возникать как у нетренированных людей, так и у профессиональных спортсменов8. А причина дискомфорта — накопление недоокисленных продуктов обмена веществ в мышечных клетках, в особенности, болезненные ощущения вызывает чрезмерное количество молочной кислоты (лактата)2. Реже причиной становится микротравма, но такое может наблюдаться, только если нарушены правила тренировки8.
Болезненность в мышцах из-за переутомления возникает не сразу, а через несколько часов или в течение 1-2 дней после тренировки или непривычной физической активности и проходит в течение недели8.
Достижение быстроты действия
Для достижения терапевтического эффекта обезболивающий препарат при боли в мышцах
должен обладать рядом характеристик – блокировать фермент циклооксигеназу, за счет чего реализуется противовоспалительное
действие
, достаточно быстро накапливаться в пораженных тканях. Благодаря таким свойствам современный обезболивающий препарат способен быстро снимать дискомфорт. Представитель данной группы лекарственных средств препарат Некст® содержит в себе комбинацию обезболивающих компонентов – ибупрофен и парацетамол, которые комплексно воздействуют на периферический и центральный механизм патогенеза боли, таким образом дополняя биологические эффекты друг друга. Некст® выпускается в лекарственной форме таблеток, покрытых пленочной оболочкой, для приема внутрь. Это обеспечивает достаточно быстрое* всасывание действующих компонентов в системный кровоток с их последующим проникновением как в очаг повреждения, так и в нервную систему. Как правило,
обезболивающие таблетки при мышечных болях
способны быстро помочь справиться с болью. Препараты на основе парацетамола и ибупрофена начинают оказывать обезболивающее действие в среднем через 15-30 минут** после приема.
Травмы
Сильная боль может возникать при разрывах мышечных волокон и сухожилий. Обычно такое случается, если нагрузка чрезмерная, а мышцы не подготовлены к ней1. Но повредить их можно также при резких движениях3. В отличие от «ломоты» при переутомлении мышц, боль вследствие травмы возникает сразу, на пике нагрузки3.
Следует помнить, что даже небольшая, но недолеченная травма может стать причиной еще более выраженного растяжения3. Поэтому при болезненных ощущениях, возникающих во время физической нагрузки, обязательно обратитесь к врачу, чтобы исключить серьезную травму.
Вернуться к началу
Особенности применения обезболивающих средств
Таблетки Некст® обладают благоприятным профилем безопасности и поэтому разрешены для безрецептурного отпуска. Для получения максимума действия, а именно снижения выраженности болевых ощущений в мышцах, важно обращать внимание на несколько рекомендаций в отношении правильного применения препарата:
- терапевтическая доза не должна превышать количество таблеток, которое указано в инструкции;
- таблетки Некст® не предназначены для лечения самого заболевания или состояния, вызывающего болезненные ощущения, они не влияют на механизм развития заболевания, , а также не устраняют воздействие причин патологического процесса. Они применяются в качестве средства симптоматической терапии – т.е. для уменьшения выраженности неприятных симптомов;
- усиление болевых или неприятных ощущений или отсутствие эффекта в течение 3-х дней является основанием для обязательного посещения врача, который назначит необходимые обследования и лечение;
Некст® – это обезболивающие таблетки при болях в мышцах
воспалительного происхождения. За счет специальной комбинации действующих веществ и лекарственной формы они помогают быстро* уменьшить выраженность болевых ощущений и снимать дискомфорт не только в мышцах, но в суставах, связках и других структурах опорно-двигательного аппарата.
* Согласно инструкции по медицинскому применению препарата Некст® ** Моллер П.Л, Синдет-Педерсен С, Петерсен С.Т. и др. Начало анальгезирующего действия ацетаминофена: сравнение перорального и инъекционного введения при постоперационной анальгезии. Британский журнал Анальгезии. Май 2005, 94(5):642-8.
Назад
Заболевания позвоночника и суставов
Мышцы реагируют на нарушение работы связанных с ними суставов4 и позвонков5. Поэтому миалгия является одним из симптомов болезней позвоночника5,11 и суставов конечностей 4. Например, при остеохондрозе или сколиозе (искривлении позвоночника) болезненность в шее, грудной клетке или пояснице связана с перенапряжением околопозвоночных мышц5,11. А в запущенных случаях, когда позвонок сдавливает нервный корешок, выходящий из спинного мозга, боль может «отдавать» в руку или ногу11.
Нередко миалгия при остеохондрозе сочетается с чувством онемения или «ползания мурашек». В момент острой боли человек застывает, принимая вынужденное положение11.
Побочные эффекты НПВС
Обсуждая применение НПВС, нужно обязательно учитывать проблему побочных эффектов.
Структурно-модифицирующие свойства НПВС проявляются при их приеме в течение длительного срока в терапевтических дозах. В этой ситуации риск развития специфических для данного класса осложнений, преимущественно в виде нарушения структуры и функции ЖКТ и сердечно-сосудистой системы (ССС), может стать основным фактором, лимитирующим терапевтический потенциал этих препаратов (табл. 1) [5]. К важнейшим осложнениям относятся так называемая НПВС-гастропатия (патология верхних отделов ЖКТ, проявляющаяся клинически выраженными язвами, кровотечением и перфорацией) и кардиоваскулярные катастрофы (инфаркт миокарда, ишемический инсульт и внезапная коронарная смерть). Наибольшее практическое значение среди данных осложнений имеет НПВС-ассоциированная гастропатия. Это является серьезной медицинской и социальной проблемой с учетом того, что НПВС широко используются [6].
Нефротоксичность является второй по значимости группой нежелательных лекарственных реакций НПВС, которая развивается вследствие системного неселективного подавления синтеза простагландинов, что приводит к сужению просвета сосудов и снижению почечного кровотока. В результате быстро развивается ишемия почек, снижается скорость клубочковой фильтрации, уменьшается объем диуреза. Происходит нарушение водно-электролитного обмена, из-за чего возникает задержка воды в организме, появляются отеки, гипернатриемия, гиперкалиемия, растет уровень креатинина в сыворотке, повышается артериальное давление. Гепатотоксичность при приеме НПВС проявляется редко. По разным оценкам, в 1–4% случаев наблюдается бессимптомное умеренное повышение уровня печеночных трансаминаз (АлАТ, АсАТ) [6].
Другие причины
Практически любое заболевание внутренних органов может привести к миалгии11. Когда какой-либо орган поражается, он создает болевые импульсы, которые частично передаются мышцам, расположенным поблизости11.
Также причиной миалгии могут быть:
- эндокринные заболевания, например, дефицит гормонов щитовидной железы16,7;
- сосудистые патологии, нарушающие питание мышц конечностей15,16;
- синдром хронической усталости7;
- нарушение баланса микроэлементов в организме16;
- прием лекарственных препаратов, снижающих уровень холестерина в крови12.
Вернуться к началу
Введение
Ноцицептивная боль — один из распространенных клинических синдромов, с которым сталкиваются врачи многих специальностей. Наибольшее применение в лечении боли получили препараты из группы нестероидных противовоспалительных средств (НПВС).
Несмотря на наличие огромного, на первый взгляд, арсенала обезболивающих средств, лечение острого и хронического болевого синдрома представляет для практикующих врачей определенные трудности из-за развития побочных эффектов. Таким образом, имеющиеся в настоящее время сведения о небезопасности длительного применения НПВС приводят к необходимости поиска и разработки новых лекарственных форм и путей их применения. Данный обзор посвящен этой актуальной проблеме и поиску путей ее решения.
НПВС давно заняли прочное место в медицинской практике и используются при различных патологиях. С клинической точки зрения они обладают некоторыми общими свойствами:
противовоспалительное действие;
болеутоляющее и жаропонижающее действие;
тормозящее влияние на агрегацию тромбоцитов;
хорошая переносимость.
Особенности миалгии
Боль, исходящая из мышц, обычно глубокая6. Острая миалгия носит защитный характер, потому что вызывает реакции, направленные на устранение повреждающего фактора11. К таким реакциям относится, например, мышечный спазм4. Но, несмотря на защитный характер, почти всегда есть риск, что боль станет хронической11. Выделяют 2 основные причины хронизации:
- Повышенная чувствительность. В ответ на раздражение в мышце выделяются вещества, поддерживающие воспаление. Они еще больше раздражают болевые рецепторы в мышцах. В ответ на частые сигналы центральная нервная система снижает болевой порог, поэтому мы можем ощущать болезненность в мышце даже при не сильном ее раздражении11.
- Спазм. При сохранении боли и спазма формируется «порочный круг»: боль вызывает спазм, а спазм поддерживает боль1,5, 11.
Механизм действия обезболивающих средств
В большинстве случаев обезболивающее при мышечной боли
представляет собой
противовоспалительный
препарат (НПВС). Механизм терапевтического эффекта заключается в том, что он блокирует функциональную активность фермента циклооксигеназы, которая отвечает за превращение арахидоновой кислоты в медиаторы воспалительной реакции простагландины (они раздражают нервные окончания, вызывая появление болевых ощущений). Выраженность противовоспалительного действия у различных представителей данной группы лекарственных средств варьирует. Также данные препараты могут выпускаться в различных лекарственных формах – таблетки,
мазь
, раствор для парентерального введения.
Препарат
Некст® содержит в своем составе комбинацию действующих компонентов, которая оказывает выраженное обезболивающее действие за счет воздействия не только на воспаление и боль в очаге повреждения, но и на центры боли в головном мозге.
Диагностика мышечной боли
Определить, почему возникла миалгия, не всегда просто. Только врач может разобраться в причинах и подобрать лечение, которое помогает избавиться от беспокоящих симптомов или облегчить их. Чтобы выяснить причину миалгии, врач проводит комплексное обследование, в том числе и неврологическое, назначает лабораторные анализы, УЗИ, компьютерную томографию и другие методы исследования3.
Лечением миалгии занимаются разные специалисты. В зависимости от ее причины, вам могут помочь травматолог, ревматолог, невролог или эндокринолог.
Выбор фармакологической терапии при спастическом мышечном гипертонусе
Основными препаратами, используемыми для снижения мышечного тонуса, являются миорелаксанты. По механизму действия различают миорелаксанты центрального действия (влияют на синаптическую передачу возбуждения в центральной нервной системе) и периферического действия (угнетают прямую возбудимость поперечно-полосатых мышц). При применении миорелаксантов могут возникать достаточно значимые побочные действия, которые при выборе препарата надо тщательно оценивать [1, 2].
При выборе антиспастических препаратов учитывают в основном их способность тормозить полисинаптические рефлексы (уменьшение спастики), оказывая при этом наименьшее влияние на моносинаптические рефлексы (сила мышц). Антиспастический препарат должен уменьшать мышечную спастичность при минимальном снижении мышечной силы [3, 4].
Медикаментозная терапия основана на использовании таблетированных и инъекционных форм. Применяемые внутрь антиспастические средства, уменьшая мышечный тонус, могут улучшить двигательные функции, облегчить уход за обездвиженным пациентом, снять болезненные мышечные спазмы, усилить действие лечебной физкультуры, предупредить развитие контрактур [5]. При легкой степени спастичности применение миорелаксантов может привести к значительному положительному эффекту, однако при выраженной спастичности могут потребоваться большие дозы миорелаксантов, применение которых нередко вызывает нежелательные побочные эффекты. Лечение миорелаксантами начинают с минимальной дозы, затем ее медленно повышают для достижения эффекта [6].
К миoрелаксантам центрального действия, наиболее часто используемым в России для лечения спастического мышечного гипертонуса, относятся баклофен, тизанидин, толперизон, диазепам [7, 8].
Баклофен (Баклосан, Лиорезал) оказывает антиспастическое действие преимущественно на спинальном уровне. Препарат представляет аналог гамма-аминомасляной кислоты (ГАМК), который связывается с пресинаптическими ГАМК-рецепторами, приводя к уменьшению выделения возбуждающих аминокислот (глутамата, аспартата) и подавлению моно- и полисинаптической активности на спинальном уровне, что и вызывает снижение спастичности. Препарат проявляет также умеренное центральное анальгезирующее действие. Баклофен используется при спинальном и церебральном спастическом мышечном гипертонусе различного генеза. Начальная доза составляет 5–15 мг/сут (в один или три приема), затем дозу увеличивают на 5 мг каждый день до получения желаемого эффекта. Препарат принимают во время еды. Максимальная доза баклофена для взрослых составляет 60–75 мг/сут. Побочные эффекты чаще проявляются седацией, сонливостью, снижением концентрации внимания, головокружением и часто ослабевают в процессе лечения. Возможно возникновение тошноты, запоров и диареи, артериальной гипертонии, усиление атаксии, появление парестезий. Требуется осторожность при лечении больных пожилого возраста, пациентов, перенесших инсульт, пациентов с язвенной болезнью желудка и двенадцатиперстной кишки. Баклофен противопоказан при эпилепсии, наличии судорог в анамнезе [9, 10].
При выраженной спастичности, когда обычное пероральное применение антиспастических препаратов не эффективно, показано интратекальное введение баклофена, которое впервые было предложено в 1984 г. R. Penn. Для достижения необходимой концентрации препарата в спинномозговой жидкости необходимо принимать довольно значительные дозы баклофена, что может привести к нарушениям сознания, сонливости, слабости. В связи с этим были разработаны системы, при помощи которых баклофен доставляется непосредственно в подоболочечное пространство спинного мозга при помощи подоболочечной баклофеновой насосной системы. При этом клинического эффекта добиваются гораздо меньшими дозами баклофена, чем при использовании таблетированных форм [11, 12].
Данная система состоит из резервуара, где содержится баклофен или аналогичный препарат, насоса (помпы), при помощи которого препарат дозированно подается в подоболочечное пространство спинного мозга через люмбальный катетер и блока питания. Из резервуара баклофен поступает непосредственно в спинномозговую жидкость, а его дозировка контролируется специальным радиотелеметрическим устройством. Количество поступающего в спинномозговую жидкость лекарственного препарата можно изменять в зависимости от клинической картины. Добавление баклофена в резервуар производится через 2–3 месяца при помощи чрезкожной пункции [13].
Использование баклофеновой помпы улучшает скорость и качество ходьбы больных с нефиксированными рефлекторными контрактурами, обусловленными высокой спастичностью мышц-синергистов и дисбалансом мышц-антагонистов. Имеющийся 15-летний клинический опыт применения баклофена интратекально у больных, перенесших инсульт, свидетельствует о высокой эффективности этого метода в уменьшении не только степени спастичности, но и болевых синдромов и дистонических расстройств. Отмечено положительное влияние баклофеновой помпы на качество жизни больных, перенесших инсульт [14].
Тизанидин (Сирдалуд) — миорелаксант центрального действия, агонист альфа-2-адренергических рецепторов. Препарат снижает спастичность вследствие подавления полисинаптических рефлексов на уровне спинного мозга, что может быть вызвано угнетением высвобождения возбуждающих аминокислот L-глутамата и L-аспартата и активацией глицина, снижающего возбудимость интернейронов спинного мозга. Тизанидин обладает также умеренным центральным анальгетическим действием. Препарат эффективен при церебральной и спинальной спастичности, а также при болезненных мышечных спазмах. Начальная доза препарата составляет 2–6 мг/сут в один или три приема, при индивидуальном подборе увеличение дозы происходит на 3–4 день на 2 мг. При пероральном приеме действие препарата проявляется через 30–45 минут, максимальный эффект наступает в течение 1–2 часов. Средняя терапевтическая доза составляет 12–24 мг/сут, максимальная доза — 36 мг/сут. В качестве побочных эффектов могут возникнуть сонливость, сухость во рту, головокружение и снижение артериального давления, что ограничивает использование препарата при постинсультной спастичности. Антиспастический эффект тизанидина сопоставим с эффектом баклофена, однако тизанидин при адекватном подборе дозировки лучше переносится, т. к. не вызывает общей мышечной слабости и не усиливает мышечную слабость в парализованной конечности [15, 16].
Толперизон (Мидокалм) — антиспастический препарат центрального действия, угнетает каудальную часть ретикулярной формации и обладает Н-холинолитическими свойствами. Толперизон снижает активность спинальных нейронов, участвующих в формировании спастичности, путем ограничения потока натрия через мембрану нервных клеток. Наиболее часто используется по 300–450 мг/сут в два или три приема. Снижение мышечного тонуса при назначении толперизона иногда сопровождается сосудорасширяющим действием, что следует учитывать при назначении больным с тенденцией к артериальной гипотонии. Также препарат может вызывать или усиливать у больных недержание мочи [17].
Основным побочным эффектом баклофена, тизанидина и толперизона является быстрое наступление мышечной слабости, причем в каждом случае врач должен находить баланс между снижением тонуса и усилением слабости. Кривая баланса между снижением спастического тонуса и усилением мышечной слабости у больных на фоне увеличения дозы Мидокалма, Сирдалуда или Баклофена показывает, что наиболее быстрое усиление слабости происходит при приеме Баклофена, а самый мягкий препарат, позволяющий эффективно подобрать индивидуальную дозировку, — Мидокалм. Во всех случаях, учитывая наличие узкого терапевтического окна, курс лечения начинают с небольшой дозы препарата, постепенно наращивая ее до достижения отчетливого антиспастического эффекта, но не до появления слабости [18, 19].
Диазепам (Реаланиум, Релиум, Сибазон) является миорелаксантом, поскольку обладает способностью стимулировать уменьшенное пресинаптическое торможение на спинальном уровне. Он не имеет прямых ГАМК-ергических свойств, увеличивает концентрацию ацетилхолина в мозге и тормозит обратный захват норадреналина и дофамина в синапсах. Это приводит к усилению пресинаптического торможения и проявляется снижением сопротивляемости растяжению, увеличением диапазона движений. Диазепам также обладает способностью уменьшать болевой синдром, вызываемый спазмом мышц. Наряду со снижением мышечного тонуса, развиваются заторможенность, головокружение, нарушение внимания и координации ввиду токсического действия на центральную нервную систему. Это значительно ограничивает применение диазепама в качестве миорелаксанта. Используется он, в основном, для лечения спастичности спинального происхождения при необходимости кратковременного снижения мышечного тонуса. Для лечения спастичности назначают в дозе 5 мг однократно или по 2 мг 2 раза в день. Максимальная суточная доза может составлять 60 мг. При больших дозах могут отмечаться расстройства сознания, преходящая дисфункция печени и изменения крови. Продолжительность лечения ограничена из-за возможного развития лекарственной зависимости [20].
Клоназепам является производным бензодиазепина. Клоназепам оказывает успокаивающее, центральное миорелаксирующее, анксиолитическое действие. Миорелаксирующий эффект достигается за счет усиления ингибирующего действия ГАМК на передачу нервных импульсов, стимуляции бензодиазепиновых рецепторов, расположенных в аллостерическом центре постсинаптических ГАМК-рецепторов восходящей активирующей ретикулярной формации ствола головного мозга и вставочных нейронов боковых рогов спинного мозга, а также уменьшения возбудимости подкорковых структур головного мозга и торможения полисинаптических спинальных рефлексов.
Быстрое наступление сонливости, головокружения и привыкания ограничивает применение этого препарата. Для снижения проявления возможных побочных реакций, достигать терапевтической дозы необходимо путем медленного титрования в течение двух недель. Для приема внутрь взрослым рекомендуется начальная доза не более 1 мг/сут. Поддерживающая доза — 4–8 мг/сут. Возможно назначение небольших доз в сочетании с другими миорелаксантами. Клоназепам эффективен при пароксизмальных повышениях мышечного тонуса. Противопоказан при острых заболеваниях печени, почек, миастении [21].
Дикалия клоразепат (Транксен) — аналог бензодиазепина, трансформируется в главный метаболит диазепама, обладает большей активностью и длительностью антиспастического действия, чем диазепам. Отмечен его хороший эффект при лечении в виде уменьшения фазических рефлексов на растяжение, обладает незначительным седативным эффектом. Первоначальная доза составляет 5 мг 4 раза в сутки, затем уменьшается до 5 мг 2 раза в сутки [22].
Дантролен — производное имидазолина, действует вне центральной нервной системы, преимущественно на уровне мышечных волокон. Механизм действия дантролена — блокирование высвобождения кальция из саркоплазматического ретикулума, что ведет к снижению степени сократимости скелетных мышц, редукции мышечного тонуса и фазических рефлексов, увеличению диапазона пассивных движений. Важным преимуществом дантролена по отношению к другим миорелаксантам является его доказанная эффективность в отношении спастичности не только спинального, но и церебрального генеза. Начальная доза — 25 мг/сут, при переносимости дозу увеличивают в течение 4 недель до 400 мг/сут. Побочные эффекты — сонливость, головокружение, тошнота, диарея, снижение скорости клубочковой фильтрации. Серьезную опасность, особенно у пожилых пациентов в дозе более 200 мг/сут, представляет гепатотоксическое действие, поэтому в период лечения надо регулярно следить за функцией печени. Элиминация дантролена на 50% осуществляется за счет печеночного метаболизма, в связи с этим он противопоказан при заболеваниях печени. Осторожность следует соблюдать и при тяжелых сердечных или легочных заболеваниях.
Катапресан — применяется в основном при спинальных повреждениях, действует на альфа-2-агонисты головного мозга, обладает пресинаптическим торможением. Из побочных эффектов отмечаются снижение артериального давления и депрессия. Первоночальная доза — 0,05 мг 2 раза в день, максимальная — 0,1 мг 4 раза в день.
Темазепам — взаимодействует с бензодиазепиновыми рецепторами аллостерического центра постсинаптических ГАМК-рецепторов, расположенных в лимбической системе, восходящей активирующей ретикулярной формации, гиппокампе, вставочных нейронах боковых рогов спинного мозга. В результате открываются каналы для входящих токов ионов хлора и таким образом потенцируется действие эндогенного тормозного медиатора — ГАМК. Рекомендуемая доза — 10 мг 3 раза в день. Эффективно его сочетание с баклофеном [23, 24].
Основные лекарственные средства, используемые для лечения спастического мышечного гипертонуса, представлены в табл.
Таким образом, выбор препарата определяется основным заболеванием, выраженностью мышечной спастичности, а также побочными эффектами и особенностями действия конкретного препарата.
Так, например, тизанидин и баклофен в большей степени действуют на тонус мышц-разгибателей, поэтому в случаях наличия значительного гипертонуса мышц-сгибателей руки, легкой спастичности мышц ноги их прием не показан, поскольку легкое повышение тонуса мышц-разгибателей ноги компенсирует мышечную слабость в ноге и стабилизирует походку больного. В таком случае средством выбора являются методы физического воздействия на мышцы верхней конечности.
При лечении церебральной спастичности наиболее часто применяют Сирдалуд, а при спинальной спастичности — Сирдалуд и Баклофен. Важным преимуществом перед другими миорелаксантами обладает Мидокалм, который не оказывает седативного эффекта и имеет благоприятный спектр переносимости, поэтому является препаратом выбора для лечения в амбулаторных условиях и для лечения пожилого контингента пациентов.
Допустима комбинация нескольких средств, что позволяет эффективно снижать тонус на меньших дозах каждого из препаратов. Сочетание препаратов с разными точками приложения, начиная от центров в головном мозге и до мышц, может привести к суммированию терапевтического эффекта.
Эффективность пероральных антиспастических препаратов снижается при их длительном использовании, часто возникает необходимость возрастающего повышения дозировок для поддержания начального клинического эффекта, что сопровождается увеличением частоты и тяжести побочных реакций [25–27].
В ситуации, когда спастичность носит локальный характер и системный эффект пероральных миорелаксантов нежелателен, предпочтительны локальные методы воздействия, одним из которых является локальное введение ботулотоксина [28, 29].
Литература
- Скоромец А. А., Амелин А. В., Пчелинцев М. В. и др. Рецептурный справочник врача-невролога. СПб: Политехника. 2000. 342 с.
- Шток В. Н. Фармакотерапия в неврологии: Практическое руководство. 4?е изд., перераб. и доп. М.: ООО «Медицинское информационное агентство», 2006. 480 с.
- Методические рекомендации по организации неврологической помощи больным с инсультами в Санкт-Петербурге / Под ред. В. А. Сорокоумова. СПб: Санкт-Петербург, 2009. 88 с.
- Леманн-Хорн Ф., Лудольф А. Лечение заболеваний нервной системы. М.: МЕДпресс-информ. 2005. 528 с.
- O’Dwyer N., Ada L., Neilson P. Spasticity and muscle contractur in stroke // Brain. 2006. Vol. 119. P. 1737–1749.
- Дамулин И. В. Синдром спастичности и основные направления его лечения // Журнал неврологии и психиатрии им. С. С. Корсакова. 2003. № 12. С. 4–9.
- Завалишин И. А., Бархатова В. П., Шитикова И. Е. Спастический парез // В кн. Рассеянный склероз. Избранные вопросы теории и практики. Под ред. И. А. Завалишина, В. И. Головкина. ООО «Эльф ИПР». 2000. С. 436–455.
- Левин О. С. Основные лекарственные средства, применяемые в неврологии: Справочник. М.: МЕДпресс-информ, 2007. 336 с.
- Бойко А. Н., Лащ Н. Ю., Батышева Т. Т. Повышение мышечного тонуса: этиология, патогенез, коррекция // Справочник поликлинического врача. 2004. Т. 4. № 1. С. 28–30.
- Дамулин И. В. Синдром спастичности и основные направления его лечения // Журнал неврологии и психиатрии им. С. С. Корсакова. 2003. № 12. С. 4–9.
- Избранные лекции по неврологии: под ред. В. Л. Голубева. М.: ЭйдосМедиа, 2006. 624 с.
- Parziale J., Akelman E., Herz D. Spasticity: pathophysiology and management // Orthopaedics. 2003. Vol. 16. P. 801–811.
- Katz R., Rymer Z. Spastic hypertonia: mechanisms and measurement // Arch. Phys. Med. Rehab. 2009. Vol. 70. P. 144–155.
- Barnes M. An overview of the clinical management of spasticity // In: Upper motor neuron syndrome and spasticity. Cambridge University Press. 2001. P. 5–11.
- Парфенов В. А. Патогенез и лечение спастичности // Русский медицинский журнал. 2011. Т. 9. № 25. С. 16–18.
- Кадыков А. С., Шахпаранова Н. В. Медикаментозная реабилитация больных со спастическими парезами. В кн.: Синдром верхнего мотонейрона. Под ред. И. А. Завалишина, А. И. Осадчих, Я. В. Власова. Самара: Самарское отд. Литфонда, 2005. С. 304–315.
- Кадыков А. С., Черникова Л. А., Сашина М. Б. Реабилитация больных с центральным постинсультным болевым синдромом // Реабилитология. Сборник научных трудов (ежегодное издание), № 1. М.: Изд-во РГМУ, 2003. С. 357–359.
- Сашина М. Б., Кадыков А. С., Черникова Л. А. Постинсультные болевые синдромы // Атмосфера. Нервные болезни. 2004. № 3. С. 25–27.
- Камчатнов П. Р. Спастичность — современные подходы к терапии // Русский медицинский журнал. 2004. Т. 12. № 14. С. 849–854.
- Гусев Е. И., Скворцова В. И., Платинова И. А. Терапия ишемического инсульта // Consilium medicum. 2003, спец. выпуск. С. 18–25.
- Кадыков А. С., Черникова Л. А., Сашина М. Б. Постинсультные болевые синдромы // Неврологический журнал. 2003. № 3. С. 34–37.
- Мусаева Л. С., Завалишин И. А. Лечение спастичности при рассеянном склерозе // Материалы 9 симпозиума «Рассеянный склероз: лечение и оздоровление». СПб: Лики России. 2000. С. 59–60.
- Инсульт. Принципы диагностики, лечения и профилактики / Под ред. Н. В. Верещагина, М. А. Пирадова, З. А. Суслиной. М.: Интермедика, 2002. 208 с.
- Sommerfeld D. K., Eek E. U.-B., Svensson A.-K. et al. Spasticity after stroke: its occurrence and association with motor impairments and activity limitations // Stroke. 2004. Vol. 35. P. 134–140.
- Bakheit A., Zakine B., Maisonobe P. The profile of patients and current practice of treatment of upper limb muscle spasticity with botulinum toxin type A // Int. J. Rehabil. Res. 2010. Vol. 33. P. 199–204.
- Малахов В. А. Мышечная спастичность при органических заболеваниях нервной системы и ее коррекция // Международный неврологический журнал. 2010. № 5. С. 67–70.
- Davis T., Brodsky M., Carter V. Consensus statement on the use of botulinum neurotoxin to treat spasticity in adults // Pharmacy and Therapeutics. 2006. Vol. 31. P. 666–682.
- Childers M., Brashear A., Jozefczyk P. Dose-dependent response to intra-muscular botulinum toxin type A for upper limb spasticity after stroke // Arch. Phys. Med. Rehab. 2004. Vol. 85. P. 1063–1069.
- Кадыков А. С. Миорелаксанты при реабилитации больных с постинсультными двигательными нарушениями // Журнал неврологии и психиатрии им. С. С. Корсакова. 1997. № 9. С. 53–55.
А. А. Королев, кандидат медицинских наук
ФГБУ «Всероссийский центр экстренной и радиационной медицины им. А. М. Никифорова» МЧС России, Санкт-Петербург
Контактная информация об авторе для переписки