Дисплазия соединительной ткани в практике врача-педиатра
Переводится с греческого как «отклонение в формировании»
Темы ДСТ «Медицинский вестник» касался уже не раз. Но до сих пор описывались лишь отдельные проявления этой врожденной патологии.
Так, в «МВ» № 21 за 2010 год профессор Л.М.Макаров рассказал о первичных каналопатиях, нередко приводящих к внезапной сердечной смерти у детей и вызываемых мутациями генов, экспрессирующихся в миокарде. В «МВ» № 4 за 2011 год профессор И.В. Викторова описала синдром гипермобильности суставов, а в № 17—18 за 2011 год профессор Э.А. Галлямов говорил о важнейшем патогенетическом факторе гастроэзофагеальной рефлюксной болезни — врожденных грыжах пищеводного отверстия диафрагмы, образующихся из-за повышенной эластичности тканей, ограничивающих это отверстие.
Уже эти публикации показывают, насколько распространены и значимы заболевания, обусловленные ДСТ. Однако многолетние исследования З.В. Нестеренко и те данные мировой науки, которые она анализирует, свидетельствуют о том, что при ДСТ поражаются не три, а гораздо больше систем организма и указанная проблема несравненно шире и острее, чем о ней думали в 1989 году, когда шотландский доктор Р. Бейтон впервые предложил обозначать врожденную патологию СТ, проявляющуюся снижением ее прочности, термином дисплазия, что в переводе с греческого обозначает «отклонение в формировании».
Если пролин изменяется на аргинин
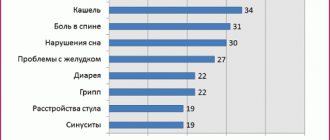
Частота выявления ДСТ (по данным разных авторов) достаточно велика — от 26 до 80 % для всех возрастов и от 74 до 85% — среди детей.
В развитии подобных дисплазий ведущее значение имеют мутации генов, кодирующих синтез и пространственную структуру коллагена и ответственных за формирование компонентов матрикса. Соответственно, согласно одной из первых классификаций ДСТ, они подразделялись на заболевания, обусловленные нарушением синтеза или катаболизма волокнистых компонентов СТ либо ее основного вещества.
Но в 1990-х годах приняли более распространенную на сегодня классификацию. К первой группе дисплазий относят достаточно редко встречающиеся дифференцированные дисплазии (ДДСТ), имеющие моногенный и определенный тип наследования, чаще — аутосомно-доминантный, и четко очерченную клиническую симптоматику. Это синдром Марфана, Элерса—Данлоса, несовершенный остеогенез и несколько других.
Чтобы ознакомиться с ДДСТ, обратимся к наиболее распространенному (частота встречаемости среди новорожденных — 5:100.000) их представителю — синдрому Марфана (СМар). Все доказанные случаи указанного синдрома — следствие мутации гена фибриллина. Он локализуется в длинном плече 15 хромосомы, поле 21 (15ql5-q21.3). Суть мутации — замена в белке фибриллина аминокислоты пролина на аргинин. В результате усиливается синтеза коллагена типа 3 и уменьшение содержания коллагена типа 1. Если в норме соотношение коллаген-1:коллаген-3 составляет 6:4, то при СМар оно падает до 3:7.
Клиническая картина в типичном случае СМар проявляется характерной триадой признаков, относящихся к скелетно-мышечной и сердечно-сосудистой системам, а также органам зрения.
Изменения скелетно-мышечной системы включают: высокий рост, астеническое телосложение (длина конечностей непропорциональна длине туловища), арахнодактилию (длинные тонкие пальцы), деформацию грудной клетки, высокое арковидное нёбо, кифосколиоз, слабость связочного аппарата. К поражениям сердечно-сосудистой системы относятся: дилатация корня аорты, аортальная регургитация, расслаивающая аневризма аорты, пролапс митрального клапана, регургитация крови при недостаточности этого клапана. Характерная патология органов зрения — иридоденез (дрожание хрусталика вследствие слабости цинновой связки), подвывих хрусталика, высокий риск отслойки сетчатки и близорукость высокой степени.
До широкого использования хирургической коррекции сердечно-сосудистой патологии практически все пациенты с СМар умирали до 30—35 лет. Причем основная группа — еще в детском возрасте. Однако в ХХI веке при адекватной терапии продолжительность жизни большинства пациентов с СМар лишь немного уступает этому показателю в общей популяции.
Высокорослые, веснушчатые, сутулые
Во вторую же группу ДСТ, составляющую расстройства, наиболее часто встречаемые практическим педиатром, включены нарушения, объединенные термином недифференцированная дисплазия (НДСТ). В отличие от дифференцированных дисплазий НДСТ — это генетически гетерогенные патологии. Основной характеристикой таких дисплазий является широкий спектр клинических проявлений без четкой симптоматики. То есть НДСТ — это не нозологическая единица, и места ей в МКБ-10 пока не нашлось. В свою очередь НДСТ делятся на 2 группы: болезни с установленным и неустановленным (а это и есть подавляющее большинство НДСТ) генным дефектом.
НДСТ у ребенка может быть диагностирована уже на этапе физикального обследования при комплексной оценке так называемых фенотипических маркеров. Выделяют внешние и висцеральные маркеры, преобладание которых зависит от того, поражение какого типа СТ имеет место — плотной или рыхлой. Критическое число внешних маркеров, позволяющее делать заключение о наличии НДСТ, сейчас принято считать за 3—6. На основании диагностической значимости отдельных признаков НДСТ предлагаются диагностические таблицы с балльной оценкой внешних и висцеральных маркеров, а также биохимических показателей.
Например, внешние изменения кожи у детей с НДСТ обычно свидетельствуют о поражении рыхлой соединительной ткани и характеризуются наличием ее гиперэластичности, повышенной растяжимости, стрий, келоидных рубцов, выраженной подкожной венозной сети, характерных пигментных пятен цвета «кофе с молоком», либо депигментации, большого количества невусов.
Зато поражения плотной СТ проявляются изменениями со стороны скелета: нарушением осанки в виде кифоза и сколиоза, сутулости, деформациями грудной клетки, плоскостопием. Такие дети, как правило, имеют высокий рост, астеническое телосложение.
У всех детей с НДСТ обнаруживаются так называемые малые аномалии развития, или дисморфии. К наиболее часто встречающимся дисморфиям относятся: светлокожесть, сросшиеся брови, широкая переносица, гипер-и гипотелоризм, голубые склеры, эпикант, неправильный рост зубов, деформированная ушная раковина, приросшая мочка, изогнутые мизинцы, неполная синдактилия пальцев, светлый или рыжий цвет волос. Диагностически значимым для выявления НДСТ является наличие у ребенка 6 и более дисморфий.
Маркеры внешние и внутренние
Обратимся теперь к внутренним маркерам НДСТ, причем подчеркнем, что между числом внешних и внутренних маркеров существует прямая корреляция.
Если говорить об интегральных показателях внутренних маркеров НДСТ, выявляемых биохимическими методами, то наиболее информативно определение уровня молекул, образующихся при распаде коллагена. Это оксипролин и гликозоаминогликаны в суточной моче, а в сывротке крови — лизин и пролин. Изменение соотношения коллагенов разных типов при НДСТ позволяет использовать в диагностике метод непрямой иммунофлюоресценции по Sternberg L.A. (1982).
На мембранах лейкоцитов обычно определяется повышенное представительство антигенов гистосовместимости HLA – А28, В35, Cw5, Cw52, а с другой стороны — сниженное количество антигенов типа А2, В12, Cw3. Наиболее перспективными, конечно, являются методы молекулярно-генетической диагностики, выявляющие конкретные генные мутации. Однако в случаях НДСТ эти анализы пока находятся на начальной стадии разработки.
Одной из наиболее часто вовлекаемых в патологический процесс при НДСТ у детей является кардиореспираторная система.
Это приводит к серьезным педиатрическим ошибкам
При НДСТ у детей еще в начале жизни нарушается формирование эластического каркаса легких, что обусловливает клапанный механизм бронхиальной обструкции и образование эмфизематозных булл из-за разрыва морфологически несостоятельных межальвеолярных перегородок. Последствием субплеврально расположенных булл может быть спонтанный пневмоторакс. Врожденный же дефект хрящевого и соединительнотканного каркаса трахеи и бронхов приводит к повышенной их подвижности, возникновению бронхоэктазов, пневмосклероза. Дискинезия трахей и бронхов приводит к развитию бронхообструктивного синдрома (БОС).
Отмечается высокая корреляционная зависимость между тяжестью течения бронхиальной астмы у детей и проявлениями дисплазий. И чем последние распространеннее и сильнее выражены, тем раньше у ребенка вдобавок к бронхиальной астме формируется легочная гипертензия и пневмофиброз.
Аномалии строения бронхолегочной системы при НДСТ ведут к ухудшению элиминации патогенных агентов в условиях измененной иммунной реактивности и способствуют длительной персистенции бактерий, формированию рецидивирующего течения пневмоний. Примечательно и то, что растет уровень атипично протекающих детских пневмоний, вызываемых внутриклеточными возбудителями — хламидиями и микоплазмами, с преимущественным поражением интерстиция легких, при рецидивирующем течении которых прогрессирует, как и в случаях астмы, пневмофиброз, легочная гипертензия.
При НДСТ нередко диагностируются и врожденные пороки: трахеобронхомегалии, трахеобронхомаляции, кистозные гипоплазии легких. На фоне дисплазий перечисленные заболевания особенно часто сопровождаются развитием тяжелых осложнений в виде пневмофиброза, легочной гипертензии, бронхоэктазов, спонтанного пневмоторакса.
К сожалению, в отличие от вышеперечисленных выраженных проявлений НДСТ у детей, субклинические варианты обычно не диагностируются. Это часто приводит к неверной трактовке патологического процесса и серьезным педиатрическим ошибкам.
Истинно малое сердце
С 1987 года в классификации заболеваний сердечно-сосудистой системы Нью-Йоркской ассоциации кардиологов был выделен синдром соединительнотканной дисплазии сердца (СДС), сопровождающий как дифференцированные, так и недифференцированные дисплазии. В свою очередь сердечные дисплазии включают несколько синдромов.
Клапанный синдром объединяет изолированные и комбинированные пролапсы клапанов сердца, миксоматозную дегенерацию клапанов. Примерно в 70% случаев синдром представлен пролапсом митрального клапана, реже — трикуспидального или аортального, расширением корня аорты и легочного ствола; эктопически расположенными хордами, аневризмами синусов Вальсальвы. В части случаев такие изменения сопровождаются явлениями регургитации, что отражается на показателях контрактильности миокарда и объемных параметрах сердца.
При торакодиафрагмальном синдроме речь идет об астенической форме грудной клетки или ее деформации, деформациях позвоночника (сколиозы, кифосколиозы, гиперкифозы, гиперлордозы), изменениях стояния и экскурсии диафрагмы. Среди детей с ДСТ наиболее часто встречается воронкообразная деформация грудной клетки, на втором месте по частоте — килевидная. Деформации грудины, ребер, позвоночника и связанное с ними высокое стояние диафрагмы уменьшают грудную полость, повышают внутригрудное давление, нарушают приток и отток крови, способствуют возникновению аритмий.
Сосудистый синдром подразумевает поражение артерий эластического типа, при котором их стенки расширяются и возникают мешотчатые аневризмы. Страдают и артерии мышечного и смешанного типов. В результате появляются бифуркационно-гемодинамические аневризмы, а также патологическая извитость сосудов вплоть до петлеобразования.
Синдром торакодиафрагмального серд-ца (СТДС) формируется параллельно прогрессированию деформации грудной клетки и позвоночника, на фоне клапанного и сосудистого синдромов. У детей с типичной астенической конституцией чаще проявляется астенический вариант СТДС. В этом случае уменьшаются размеры камер сердца, но при сохранении их нормальной толщины. Словом, идет формирование «истинного малого сердца», функционирующего без серьезных отклонений.
К сожалению, у части детей с деформацией грудной клетки при смещении сердца, когда оно «уходит» от механических воздействий костяка грудной клетки, ротируя и сопровождаясь «перекрутом» основных сосудистых стволов, формируется так называемый ложностенотический вариант СТДС, протекающий особенно тяжело.
Синдром метаболической кардиомиопатии объединяет кардиалгии, аритмии, нарушения процессов реполяризации. Развитие метаболической кардиомиопатии определяется влиянием кардиальных факторов (клапанный синдром, варианты СТДС) и экстракардиальных условий (вегетативные дисфункции, дефицит микро- и макроэлементов и др.). Кардиомиопатии при ДСТ обычно не имеют специфических симптомов.
Аритмический синдром включает желудочковые и предсердные экстрасистолии, пароксизмальные тахиаритмии, миграции водителя ритма, атриовентрикулярные и внутрижелудочковые блокады, аномалии проведения импульса по дополнительным путям, синдром предвозбуждения желудочков, синдром удлинения интервала Q-T.
Практический педиатр должен помнить о том, что у детей, страдающих ДСТ, кардиомиопатии и аритмический синдром встречаются очень часто (у 60—64% пациентов). И именно они определяют повышенный риск внезапной сердечной смерти таких детей.
Универсальное средство еще не найдено
Универсальное средство, восстанавливающее соединительную ткань при любых формах дисплазий, еще не найдено. Для каждого ребенка с ДСТ подбирается индивидуальная программа лечения. Три ее основные задачи: улучшение обменных процессов соединительной ткани, устранение уже возникших осложнений и профилактика новых.
В любом случае речь идет о фактически согласованной работе бригады педиатров нескольких специальностей. И об очень сложном, комплексном лечении, которое затрагивает весь детский период жизни (в РФ — до 18 лет). Успеем привести лишь один пример такой терапии, относящийся к синдрому Марфана.
Немедикаментозная терапия включает строгое соблюдение ребенком режима, в том числе питания, где акцент делается на потреблении полноценных белков и продуктов, содержащих полиненасыщенные жирные кислоты; и физической активности, отдельные виды которой таким пациентам запрещены. Существует перечень профессий, к которым нельзя готовить школьников, страдающих ДСТ.
Лекарственное лечение включает симптоматическое назначение b-адреноблокаторов. В случае расширения аорты, и особенно при наличии регургитации, они уменьшают выброс в аорту и соответственно нагрузку на ее стенки, корригируя сопутствующую гипертензию. Считается, что эти кардиотропные средства снижают риск внезапной смерти у детей с поражениями сердца при СМар и любых других ДСТ.
Поскольку доказано, что прогрессирование скелетных патологий при синдроме Марфана замедляется при устранении дефицита микроэлементов (кальций, магний, цинк, медь), необходимых для формирования СТ, в терапии используются пищевые добавки, содержащие вышеперечисленные вещества, а также гиалуроновую кислоту, синтетические аналоги витаминов К и D3. В крови больных с СМар нередко отмечается повышенный уровень соматотропного гормона. Поэтому для уменьшения его секреции с раннего детства назначают высокожировые энпиты класса Омега-3 в питании.
Обратимся теперь к терапии с воздействием на соединительную ткань. Она включает аскорбиновую кислоту в виде специальных детских молочных коктейлей, а также корректоры нарушения синтеза и катаболизма гликозаминогликанов — хондроитинсульфат и янтарную кислоту. Еще один препарат, рекомендуемый как корректор биоэнергетических процессов, это карнитина хлорид.
Что могут сделать хирурги
При аневризме аорты, расслаивающей аневризме, пороке аортального клапана с симптомами сердечной недостаточности, детям с синдромом Марфана может помочь только оперативное лечение. Разработаны четкие показания для протезирования. Например, аневризматически расширенная аорта обязательно заменяется эндо- или экзопротезом. При пролапсе митрального клапана, сопровождающемся «стабильной» регургитацией протезирование клапана не проводят. Однако при быстром прогрессировании регургитации, вплоть до присоединения левожелудочковой недостаточности, замена клапана становится необходимой.
Оперативное лечение деформаций грудной клетки и позвоночника является крайне травматичной процедурой, проводимой в несколько этапов, нередко осложняющейся плевритами, перикардитами, пневмониями. Вопрос о ее целесообразности многократно обсуждался на симпозиумах, посвященных ДСТ.Специалисты различных стран приняли единую позицию, отрицающую целесообразность таких операций при любых ДСТ.
Основные причины дисплазий
Внутренние причины:
- семейная предрасположенность к дисплазии
- наследственные изменения
Внешние причины:
факторы, воздействующие на организм женщины во время беременности
- физические и химические агенты
- некоторые лекарственные средства (группа антибиотиков тетрациклинового ряда)
- вредные факторы на производстве
- плохая экология
- вредные привычки
- воздействие ядов, токсинов
- вирусные заболевания во время беременности
- токсикозы беременности
- неполноценное питание, с недостатком минералов, витаминов.
В результате воздействия вредных факторов во время беременности происходит нарушение развития, формирования костей, связок и мышц коленного сустава.
История
Научный и практический интерес к гипермобильности суставов возник еще в конце XIX века, когда были описаны наследственные синдромы, в клинической картине которых гипермобильность суставов являлась одним из ведущих симптомов. Врачи различных специальностей регулярно видели пациентов, у которых имеет место структурное невоспалительное поражение (часто врожденное или проявляющееся в молодом возрасте) отдельных органов или систем.
Группа наследственных заболеваний соединительной ткани и скелета была впервые выделена американским генетиком Mc Kusick в 1955 году. К тому времени она объединяла лишь некоторые нозологические формы: несовершенный остеогенез, синдром Марфана, синдром Элерса-Данло, эластическую псевдоксантому и гаргоилизм.
В 1967 году Кирк (J. H. Kirk), Анселл (B. M. Ansell) и Байватерс (E. G. Bywaters) предложили термин «гипермобильный синдром» для характеристики патологии у пациентов с гиперподвижными суставами и стойкими жалобами со стороны опорно-двигательного аппарата при отсутствии у них признаков какого-либо другого ревматического заболевания. С этого времени началось систематическое изучение указанной патологии в рамках ревматологических синдромов. Термин «гипермобильный синдром» отражал феномен гипермобильности суставов, сочетающийся с дисфункцией опорно-двигательного аппарата (подвывихи, артралгии).
Сегодня, благодаря достижениям генетики были описаны и классифицированы свыше 200 заболеваний соединительной ткани и скелета наследственного характера.
- Гипермобильная кисть
- Гипермобильный пястно-фаланговый сустав I пальца
- Гипермобильная кисть
- Гипермобильная кисть
- Гипермобильная лодыжка
- Гипермобильное плечо
- Гипермобильный палец
- Гипермобильные лопатки
- Гипермобильные локтевые суставы
Содержание
- 1 История
- 2 Терминология
- 3 Патогенез
- 4 Классификация
- 5 Клинические проявления 5.1 Синдром неврологических нарушений
- 5.2 Астенический синдром
- 5.3 Клапанный синдром
- 5.4 Торакодиафрагмальный синдром
- 5.5 Сосудистый синдром
- 5.6 Торакодиафрагмальное сердце
- 5.7 Аритмический синдром
- 5.8 Синдром внезапной смерти
- 5.9 Бронхолегочный синдром
- 5.10 Висцеральный синдром
- 5.11 Синдром патологии органа зрения
- 5.12 Геморрагические гематомезенхимальные дисплазии
- 5.13 Синдром патологии стопы
- 5.14 Синдром гипермобильности суставов
- 5.15 Вертеброгенный синдром
- 5.16 Косметический синдром
- 5.17 Нарушения психической сферы
Классификация
Классификация ДСТ — один из самых дискуссионных научных вопросов. Отсутствие единой, общепринятой классификации ДСТ отражает разногласие мнений исследователей по данной проблеме в целом. ДСТ может классифицироваться с учетом генетического дефекта в периоде синтеза, созревания или распада коллагена. Это перспективный классификационный подход, который дает возможность обосновать генетически дифференцированную диагностику ДСТ, однако на сегодняшний день данный подход ограничен наследственными синдромами ДСТ.
Т. И. Кадурина выделяет MASS-подобный фенотип, марфаноидный и элерсоподобный фенотипы, отмечая, что именно эти три фенотипа являются наиболее частыми формами несиндромной ДСТ. «Марфаноидный фенотип» характеризуется сочетанием «признаков генерализованной дисплазии соединительной ткани с астеническим телосложением, долихостеномелией, арахнодактилией, поражением клапанного аппарата сердца (а порой и аорты), нарушением зрения». При «Элерсоподобном фенотипе» о. «MASS-подобному фенотипу» присущи «признаки генерализованной дисплазии соединительной ткани, ряд нарушений со стороны сердца, скелетные аномалии, а также кожные изменения в виде истончения или наличия участков субатрофии». На основе этой классификации предлагается формулировать диагноз ДСТ.
Строение суставов
Любой сустав является соединением двух или трех костей. Поверхности костей, входящих в сустав, покрыты суставным хрящом. Это обеспечивает подвижность в суставе. В суставе имеется узкий просвет между суставными эпифизами – суставная щель. Снаружи сустав покрыт специфической оболочкой – суставной сумкой. Изнутри эта сумка выстлана синовиальной оболочкой, которая вырабатывает синовиальную жидкость. Это своеобразная смазочная жидкость. Она обеспечивает скольжение и облегчает движение в суставе.
Строение коленного сустава
В образовании коленного сустава участвуют большеберцовая и бедренная кости. Своими суставными концами – эпифизами, они образуют сустав. Он покрыт синовиальной оболочкой. Внутри коленного сустава находятся крестообразные связки и мениски. Мениск – специфическое хрящевое образование. Он является амортизаторов и обеспечивает лучшее сопоставление суставных поверхностей.
Связки коленного сустава
По наружной поверхности сустава располагается мощный связочный аппарат. Мениски и связки коленного сустава обеспечивают стабильность сустава, способствуют его устойчивости к нагрузкам. Наружные боковые связки препятствуют разболтанности движений, увеличивает сопротивление к ударам и толчкам.
Все связки и капсула сустава обеспечивают его стабильное функционирование и целостность сустава.
Надколенник
В переднем отделе сустава расположен надколенник – коленная чашечка. Это отдельная кость, расположена в сухожилии четырехглавой мышце бедра. Задней своей поверхностью соприкасается с большеберцовой костью. Надколенник подвижен. Его можно сдвинуть вверх, вниз, в стороны.
Боковая рентгенограмма правого коленного сустава.
- бедренная кость
- бедренная кость
- медиальный мыщелок большеберцовой кости
- латеральный мыщелок большеберцовой кости
- малоберцовая кость, головка
- малоберцовая кость
- большеберцовая кость
- бугристость большеберцовой кости
- мыщелок бедренной кости, наружный
- мыщелок бедренной кости, внутренний
- надколенник
Мягкотканные элементы коленного сустава
К мягкотканым элементам коленного сустава относятся в первую очередь мышцы, прикрепляющиеся своими сухожилиями к суставу:
- четырехглавая мышца бедра всеми своими частями прикрепляется к большеберцовой кости, к ее бугристости
- связка надколенника, соединяет его с бугристостью большеберцовой кости
- портняжная мышца
- тонкая мышца
- большая приводящая мышца
- двуглавая мышца бедра
- полусухожильная мышца
- полуперепончатая мышца
- трехглавая мышца голени
- подколенная мышца.
Все эти мышцы обеспечивают движения коленного сустава и его функцию.
Так же к мягкотканым элементам относятся сухожильно – связочный аппарат и суставная капсула сустава.
Признаки дисплазии коленного сустава
В первую очередь, это особенности изменения анатомического строения коленного сустава. Дисплазия коленного сустава может проявляться:
- Неправильной формой эпифизов костей
- Сглаженностью суставных поверхностей
- Сужением или неравномерностью просвета суставной щели
- Заострением межмыщелковых возвышений большеберцовой кости
- Изменением взаиморасположения суставных концов
- Изменение формы надколенника, смещение надколенника
- Несовпадение поверхностей надколенника и большеберцовой кости.
Все эти диспластические изменения приводят к усилению нагрузки на хрящи и на отдельные участки суставных поверхностей. Нагрузка распределяется неравномерно. Способствуют преждевременному стиранию хрящевого покрова. Может образоваться деформации сустава. В дальнейшем может развиться деформирующий артроз.
Довольно часто в интернете можно встретить определение дисплазии коленного сустава, как изменение расположения надколенника или изменение его формы. Это довольно упрощенное понимание дисплазии коленного сустава. При данной патологии могут наблюдаться отклонения в строении всех элементов сустава.
Патогенез
ДСТ морфологически характеризуется изменениями коллагеновых, эластических фибрилл, гликопротеидов, протеогликанов и фибробластов, в основе которых лежат наследуемые мутации генов, кодирующих синтез и пространственную организацию коллагена, структурных белков и белково-углеводных комплексов, а также мутации генов ферментов и кофакторов к ним. Некоторые исследователи, основываясь на выявляемом в 46,6-72,0 % наблюдений при ДСТ дефиците магния в различных субстратах (волосы, эритроциты, ротовая жидкость), допускают патогенетическое значение гипомагниемии.