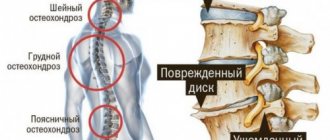
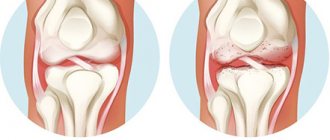
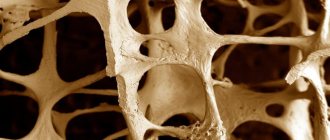
Признаки подагры
Боли при подагре – основные симптомы, как правило, это болезненные ощущения в суставах пальцев, стоп, локтей, колен и других. Как раз в этом и заключается вся сложность, ведь это симптомы многочисленных ревматологических заболеваний. Этим обстоятельством объясняется сложность диагностики. Чтобы определиться с диагнозом, врачи опираются на внешние проявления болезни, а также на данные лабораторных и инструментальных методов диагностики. Диагностика и ее сложность во многом зависит от выраженности клинической картины, а также причин, спровоцировавших развитие болезни. Осмотр, сбор анамнеза, инструментальные и лабораторные методы диагностики позволят обнаружить:
- гиперурикемию – повышенный уровень мочевой кислоты, и это основная причина, приводящая к болезни и провоцирующая симптомы;
- накопление кристаллов соли (уратов), в том числе и в тканях, окружающих суставы;
- воспалительную реакцию, которая и вызывает сильную боль.
Если заболевание существует длительно, то поражаются и почки, поэтому оценка их работы и раннее выявление сбоев – один из обязательных пунктов в обследовании.
Осложнения без должного лечения
Отсутствие лечения на ранних стадиях практически всегда приводит к осложнениям. Они могут появиться через годы и даже при бессимптомной форме заболевания.
Подагрические нерастворимые узлы (тофусы) откладываются в других суставах или околосуставных тканях, начинается воспалительный процесс. Развивается хронический подагрический артрит, при котором повреждаются суставные хрящи и связки, суставы разрушаются, деформируются кости. Человек теряет способность нормально передвигаться, боли становятся постоянными.
Уратные соли могут откладываться в почках, приводя к мочекаменной болезни, нефропатии и подагрическому нефриту. Со временем возможна почечная недостаточность. Почки не справляются с работой, что становится причиной стойкой артериальной гипертензии.
Начало обследования: опрос
Боль в суставах, плохое самочувствие – симптомы, при которых необходима консультация врача-ревматолога. Признаки, которые характерны для болезни, не являются специфичными, поэтому нужна сложная и длительная диагностика. И важную роль в этом вопросе имеет выяснение жалоб и анамнез.
Что беспокоит пациента, когда появились первые симптомы, что им предшествовало и главное – как они развивались. Были ли боли в суставах в прошлом: как давно, какие суставы были поражены. Учитывая наследственный фактор, обязательно нужно определить семейную историю болезни, а также наличие вредных привычек: курение, злоупотребление алкоголем и др. Важно выяснить, какое количество воды употребляет человек в сутки, был ли длительный прием лекарственных препаратов и каких именно, а также болезни почек, которые могут повлиять на их фильтрующие способности.
Развитие клинической картины
Сбор анамнеза и осмотр позволяют в некоторых случаях поставить предварительный диагноз, еще до проведения лабораторных и инструментальных методов обследования. При внешнем осмотре врач оценивает наличие воспалительного процесса в суставах и окружающих его тканях, подвижность сустава, амплитуду его движений. Регулярные осмотры у врача необходимы для оценки клинической картины, ее развития, для постановки диагноза и, конечно, назначения лечения подагры.
Инструментальные методы обследования
Вычислить причину болей в суставах и тканях, окружающих его, помогут некоторые виды аппаратного обследования. Появление симптомов – повод для проведения УЗИ, КТ и рентгенографии. При этом стоит помнить, что на ранних стадиях развития болезни эти методы обследования малоэффективны, поскольку деструктивные процессы в тканях не выражены. Выявить ревматологические заболевания помогут инструментальные методы обследования. При назначении инструментальной диагностики учитываются следующие нюансы:
- УЗИ наиболее информативно на 3-4 день после острого приступа. Исследование выявит деструктивные изменения в суставе, отек и уплотнение мягких тканей. Но позднее УЗИ малоэффективно.
- КТ поможет выявить тофусы. Этот метод обследования наиболее информативен на поздних стадиях болезни, когда образуются кристаллы соли в околосуставных тканях. На ранних стадиях подагры КТ позволяет определить уплотнение околосуставных тканей.
- Рентгенография на ранних стадиях болезни проводится с целью исключения других ревматологических болезней. Если же диагноз выставлен, то проводится только при хроническом течении болезни для оценки структурных изменений и состояния суставов.
- Сцинтиграфия – метод визуализации. В кровь вводятся радиоактивные изотопы, что позволяет с высокой точностью определить места, где произошло отложение солей. Этот метод обследования выявляет болезнь даже на ранних стадиях, когда образование уратов только начинается.
Какие анализы нужны?
Лабораторные анализы проводятся даже на ранних стадиях. Причем удается вычислить не только болезнь на ранних стадиях, но и предрасполагающие факторы для ее развития. При помощи лабораторной диагностики проводится так называемый дифференциальный диагноз, то есть отличие одной болезни от другой. Общий анализ крови
– обязательное обследование, которое наиболее информативно при острых приступах болезни.
Биохимический анализ крови
покажет повышенную концентрацию мочевой кислоты. Этот же метод обследования выявит повышенную концентрацию С-реактивного белка, кальция, а также повышенную концентрацию липопротеинов, липидов и др.
Общий анализ мочи
назначается в обязательном порядке, хотя и проводится с целью оценки работы почек. Оценивается количество мочевой кислоты, которая выводится почками. Здесь существует интересная закономерность: при патологических процессах в почках объем мочевой кислоты, которая выводится с мочой, как правило, минимален. На основании полученных данных выставляется диагноз, разрабатывается тактика лечения: диета, лекарства от подагры, физиотерапевтические методы лечения и др. Лечить подагру может только врач с учетом всевозможных нюансов, клинической картины и, конечно, причин формирования. В следующих материалах мы продолжим разговор о лечении болезни.
Текст: Юлия Лапушкина.
Кардиоваскулярный риск у больных подагрой и возможные пути его снижения
Подагра — системное заболевание, при котором в различных тканях откладываются кристаллы моноурата натрия и у лиц с гиперурикемией развивается воспаление, обусловленное внешнесредовыми и/или генетическими факторами [1]. Распространенность подагрического артрита в популяции достаточно высока и составляет 5–28 на 1000 мужчин и 1–6 на 1000 женщин, а число новых случаев в год — 1–3 на 1000 мужчин и 0,2 на 1000 женщин [2].
За последние десятилетия заболеваемость подагрой увеличилась в несколько раз [3]. Несмотря на подробное описание подагры уже в прошлом тысячелетии, данное заболевание остается одним из поздно диагностируемых процессов. По данным клиники терапии и профболезней им. Е. М. Тареева Первого МГМУ им. И. М. Сеченова, из 128 больных типичной подагрой более чем у половины диагноз был установлен крайне поздно, уже при далеко зашедшем поражении органов [4].
Интерес к проблеме подагры обусловлен не только ростом ее заболеваемости, но и обнаруженными взаимосвязями подагры, гиперурикемии и кардиоваскулярного риска [5]. Гиперурикемия играет важную роль в развитии артериальной гипертензии (АГ), сахарного диабета и является независимым предиктором сердечно-сосудистых заболеваний [6].
Патогенетические механизмы повышения сердечно-сосудистой заболеваемости и смертности у лиц с гиперурикемией и подагрой многообразны. Хроническое воспаление — один из факторов, который запускает и поддерживает процесс формирования атеросклеротической бляшки у больных с гиперурикемией и подагрой [7]. Окислительный стресс является еще одним из важных факторов, способствующих эндотелиальной дисфункции и повреждению сосудистой стенки, лежащих в основе развития сердечной недостаточности (СН), АГ, ишемической болезни сердца (ИБС) у больных ревматическими заболеваниями [8].
По нашим данным, совпадающим с данными литературы [9], пациенты с подагрой относятся к группе больных с высоким риском фатальных сердечно-сосудистых осложнений, что обусловлено имеющейся эндотелиальной дисфункцией (повышением антитромбогенной активности сосудистой стенки, повреждением сосудистой стенки, увеличением жесткости артерий). Традиционные факторы сердечно-сосудистого риска чаще встречаются у больных подагрой, чем в общей популяции. В нашем исследовании у 91% больных по данным суточного мониторирования артериального давления (АД) выявлялась АГ, у большинства больных подагрой (73,7%) выявлен суточный профиль с недостаточной степенью ночного снижения АД (non-dipper) [10]. У таких пациентов значительно повышена жесткость артерий, уровень С-реактивного белка (СРБ) (р < 0,05) [11].
В последние годы исследователи находят взаимосвязь также между наличием аортального стеноза и подагры, однако является ли подагра фактором риска либо маркером поражения клапанов сердца, еще только предстоит изучить [12]. Но несомненно, что поражение сердечно-сосудистой системы при подагре, наряду с артритом, является одним из основных клинических проявлений подагры, определяющим тяжесть течения и прогноз заболевания [13]. Сердечно-сосудистая заболеваемость и смертность превышают смертность от поражения почек у больных подагрой [14].
В качестве иллюстрации приводим клинический случай пациента с подагрой с развитием фатального сердечно-сосудистого осложнения.
Пациент К., 62 лет, житель Саратовской области, работал в течение 38 лет водителем. Страдал подагрой в течение 13 лет. Заболевание началось типично, с возникновения острых приступов артрита суставов стоп, включая первые плюснефаланговые суставы, суставы предплюсны, повторяющихся 3–4 раза в год. Приступы купировались приемом нестероидных противовоспалительных препаратов (НПВП) в течение нескольких дней. Через 3 года от начала заболевания обратился к ревматологу, выставлен диагноз подагры, назначен аллопуринол в дозе 200 мг/сутки, но пациент изначально демонстрировал низкую приверженность лечению. Аллопуринол принимал только лишь при рецидиве артрита, совмещал с приемом НПВП. Частота приступов артрита непрерывно увеличивалась, в течение последних 8 лет не было межприступных периодов. С 56-летнего возраста наблюдался максимально быстрый рост подкожных тофусов, что привело к деформации, обезображиванию конечностей, выраженному ограничению объема движений в суставах (кистей, стоп, коленных, голеностопных, лучезапястных, локтевых, плечевых). С 58 лет периодически отмечал повышение АД (максимально до 170 и 100 мм рт. ст.), однако постоянной антигипертензивной терапии не получал. Эпизодически принимал эналаприл 20 мг в сутки.
Был госпитализирован в ревматологическое отделение областной клинической больницы в апреле 2015 г. При осмотре: рост — 178 см, масса тела — 109 кг, ИМТ — 34,4 кг/м2.
Обращали на себя внимание подкожные образования (тофусы) в области ушных раковин, тыльной поверхности пальцев стоп, локтевых, коленных суставов, кистей, некоторые — больших размеров (рис.); болезненность, припухлость суставов кистей и стоп, голеностопных, коленных суставов; ограничение движений в них. Интенсивность боли в суставах по визуальной аналоговой шкале — 80 мм. По данным лабораторных исследований: сывороточный уровень мочевой кислоты (МК) крови — 740 мкмоль/л (целевой уровень 360 мкмоль/л), креатинина — 98,4 мкмоль/л, СРБ — 10,4 мг/л, СОЭ — 45 мм/ч. После купирования артрита была возобновлена терапия аллопуринолом 200 мг/сутки. Через 1 неделю после начала терапии сывороточный уровень МК снизился до 504,3 мкмоль/л. Из антигипертензивных препаратов пациент принимал лозартан 100 мг/сутки, амлодипин 5 мг/сутки. На этом фоне АД было в пределах 140 и 90 мм рт. ст. Пациент был выписан на амбулаторный этап с рекомендациями продолжить терапию, титровать дозу аллопуринола до достижения целевых значений МК, чего пациент не выполнял. Терапию получал нерегулярно.
В феврале 2021 г. по экстренным показаниям был госпитализирован в отделение неотложной кардиологии с клиникой острого коронарного синдрома. Несмотря на проводимую терапию в полном объеме, больной скончался через 14 часов после поступления в стационар от острого Q-инфаркта миокарда с локализацией в задней стенке левого желудочка.
Данное клиническое наблюдение не уникально, а скорее типично. Пациенты мужского пола среднего и пожилого возраста, имеющие метаболический синдром, тофусную подагру, без адекватной гиперурикемической терапии чрезвычайно часто погибают от сердечно-сосудистых осложнений.
В 2021 г. были опубликованы новые Европейские рекомендации по ведению пациентов с подагрой [15]. Одной из причин пересмотра ранее существующих рекомендаций явилось появление новых лекарственных препаратов. Так, в последние десятилетия для лечения острых приступов, наряду с НПВП и колхицином, стали применяться ингибиторы ИЛ-1, в качестве уратснижающих препаратов — непуриновые ингибиторы ксантиноксидазы (КОИ), урикозурики, препараты уриказы.
В нашей стране ингибиторы ксантиноксидазы представлены двумя классами препаратов — пуриновыми (аллопуринол, оксипуринол) и непуриновыми (фебуксостат, топироксостат).
Согласно последним рекомендациям, аллопуринол остается препаратом первой линии уратснижающей терапии при сохраненной функции почек. Если целевой уровень МК не может быть достигнут с помощью адекватной дозы аллопуринола, то препарат должен быть заменен на фебуксостат. Фебуксостат показан при непереносимости аллопуринола и является препаратом выбора при хронической болезни почек [15].
Фебуксостат недавно зарегистрирован в Российской Федерации. Первый опыт его применения в нашей стране демонстрирует возможность его использования у больных с тяжелой инвалидизирующей подагрой [16]. До последнего времени отсутствие альтернативы аллопуринолу практически не оставляло шансов добиться желаемого результата лечения и предотвратить прогрессирование подагры, развитие осложнений, связанных с подагрой и гиперурикемией [17].
Важным аспектом изучения эффективности современных препаратов представляется влияние противоподагрических препаратов на сердечно-сосудистый риск. Предварительные сообщения о применении канакинумаба с целью профилактики сердечно-сосудистых заболеваний в рамках исследования CANTOS (Canakinumab ANti-inflammatory Thrombosis Outcomes Sudy), проводимого для проверки воспалительной теории атеросклероза, результаты других исследований предполагают благоприятное влияние препарата на исходы, связанные с атеросклерозом, что принципиально важно для пациентов с подагрой [18].
В результате крупных исследований были получены доказательства того, что эффективная уратснижающая терапия не только уменьшает риск развития новых приступов артрита и повышает качество жизни пациентов, но и снижает риск сердечно-сосудистых заболеваний, поражения почек и смертность [19].
В литературе имеются противоречивые данные в отношении протективного действия КОИ на сердечно-сосудистую систему [20]. Популяционное исследование в Великобритании показало, что прием аллопуринола при подагре отождествлялся с 19% снижением риска смерти [21]. Имеются данные о снижении выраженности эндотелиальной дисфункции на фоне приема аллопуринола у больных с высоким кардиоваскулярным риском [22].
В литературе обсуждается вопрос о возможном дозозависимом эффекте влияния аллопуринола на сердечно-сосудистый риск. Так, в работе А. Noman с соавт. (2010) аллопуринол в высоких дозах (600 мг/сутки) у пациентов со стенокардией показал себя в качестве эффективного антиишемического средства, а у пациентов с сердечной недостаточностью те же высокие дозы препарата двукратно снижали смертность [23]. Тогда как в более поздних работах имеется указание на нивелирование позитивного кардиоваскулярного эффекта аллопуринола в дозе, превышающей 300 мг в сутки [24], что может быть связано с повышением оксидативного стресса в условиях высокой концентрации метаболита аллопуринола — оксипуринола [25].
В 2021 г. в работе M. Bredemeier с соавт. представлен систематический обзор и метаанализ рандомизированных исследований [26], целью которого явился анализ случаев основных неблагоприятных сердечно-сосудистых событий, смертности (общей и сердечно-сосудистой) в рандомизированных контролируемых исследованиях с применением КОИ по сравнению с плацебо или отсутствием лечения. Анализ включал 81 статью (10 684 больных, 6434 пациенто-лет). Результаты показали, что назначение КОИ существенно не влияло на риск основных неблагоприятных сердечно-сосудистых событий (относительный риск (ОP) 0,71, 95% доверительный интервал (ДИ) 0,46–1,09) и смерти (ОР 0,89, 95% ДИ 0,59–1,33), но приводило к снижению риска общего числа (ОР 0,60, 95% ДИ 0,44–0,82), в том числе серьезных, сердечно-сосудистых событий (ОР 0,64, 95% ДИ 0,46–0,89) и АГ (ОР 0,54, 95% ДИ 0,37–0,80). Это касалось и больных с наличием сердечно-сосудистой патологии в анамнезе (ОР 0,42, 95% ДИ, 0,23–0,76).
У больных, получающих аллопуринол, был ниже риск развития инфаркта миокарда (ОР 0,38, 95% ДИ 0,17–0,83), АГ (ОР 0,32, 95% ДИ 0,18–0,58), общего числа (0,48, 0,31–0,75) и серьезных сердечно-сосудистых событий (ОР 0,56, 95% ДИ 0,36–0,86). Однако этот эффект нивелировался при повышении дозы аллопуринола выше 300 мг/сутки, что требует дальнейших исследований.
Кардиоваскулярные эффекты непуриновых ингибиторов ксантиноксидазы менее изучены. В результате селективного ингибирования двух форм ксантиноксидазы (окисленной и восстановленной) при приеме фебуксостата происходит снижение концентрации МК в сыворотке крови больного.
Описано влияние фебуксостата на инсулинорезистетнность (ИР), экспрессию высокочувствительного СРБ (вч-СРБ), что является важным как в терапии подагры, так и в снижении кардиоваскулярного риска [27]. В исследование J. Meng с соавт. было включено 42 пациента с подагрой и 20 испытуемых группы контроля, сопоставимых по полу и возрасту. Определяли уровень инсулина и глюкозы крови натощак, вч-СРБ. ИР оценивали с использованием индекса HOMA-IR. У пациентов с подагрой были более высокие показатели МК, инсулина, индекс НОМА-Ш и уровень вч-СРБ, чем у лиц группы контроля (р < 0,05). После 4, 12 и 24 недель лечения фебуксостатом концентрация МК и вч-СРБ значительно снизилась (р < 0,05). Уровень инсулина и индекс НОМА-IR несколько снизились после 4 недель терапии и значительно уменьшились через 12 и 24 недели лечения. Таким образом, фебуксостат позволяет эффективно контролировать уровень МК в сыворотке и повышает чувствительность к инсулину у пациентов с подагрой.
Непуриновые ингибиторы ксантиноксидазы обладают антиоксидантными свойствами за счет сокращения числа метаболитов пуринового метаболизма, улучшения функции эндотелия [28]. Существуют исследования, предполагающие преимущества фебуксостата перед аллопуринолом по устранению эндотелиальной дисфункции [28] и даже улучшение показателей у пациентов, получавших фебуксостат, по сравнению с аллопуринолом [29]. В то же время, согласно инструкции по медицинскому применению фебуксостата, применение препарата не рекомендуется у пациентов с ИБС или застойной СН, поскольку, согласно результатам долгосрочных широкомасштабных исследований, в группе пациентов, получающих фебуксостат, по сравнению с группой пациентов, получающих аллопуринол, отмечалось увеличение количества нарушений со стороны сердечно-сосудистой системы [30]. В группе фебуксостата отмечалось численно больше сердечно-сосудистых событий по композитной конечной точке «нефатальный инфаркт миокарда, нефатальный инсульт или сердечно-сосудистая смерть». Однако эти различия с группами аллопуринола не достигли статистической достоверности и не повторились в исследовании CONFIRMS [31].
В настоящее время продолжаются рандомизированные клинические исследования, способные оценить влияние фебуксостата на сердечно-сосудистый риск у больных с подагрой [32].
Таким образом, у больных подагрой повышен кардиоваскулярный риск. Адекватная уратснижающая терапия способна не только нормализовать уровень МК крови, но и улучшить жизненный прогноз пациентов с подагрой за счет снижения риска развития сердечно-сосудистых заболеваний. В представленном нами клиническом наблюдении отсутствие адекватной уратснижающей терапии явилось одним из факторов развития неблагоприятного исхода. Для уточнения механизмов и особенностей влияния различных ингибиторов ксантиноксидазы на сердечно-сосудистый риск требуются дальнейшие исследования.
Литература
- Ревматология. Национальное руководство / Под ред. Е. Л. Насонова. М.: ГЭОТАР-Медиа, 2008. 372 с.
- Барскова В. Г., Насонова В. А. Подагра: клиническое течение, диагностика, лечение. Качество жизни // Медицина. 2003. № 3. С. 49–53.
- Arromdee E., Michet C. J., Crowson C. S. Epidemiology of gout: is the incidence rising? // J. Rheumatol. 2012; 29: Р. 2403–2406.
- Мухин Н. А. Подагра: лики болезни // Современная ревматология. 2007. № 1. С. 5–9.
- Елисеев М. С., Денисов И. С., Маркелова Е. И. и др. Независимые факторы риска развития тяжелых сердечно-сосудистых осложнений у мужчин с подагрой: результаты 7-летнего проспективного наблюдения // Терапевтический архив. 2021. № 89 (5). С. 10–19.
- Feig D. I., Kang D. H., Johnson R. J. Uric acid and cardiovascular risk // N. Engl. J. Med. 2008; 359 (17): P. 1811–1821.
- Perez-Ruiz F., Becker M. A. Inflammation: a possible mechanism for a causative role of hyperuricemia/gout in cardiovascular disease // Curr. Med. Res. Opin. 2015; 31. Suppl 2: 9–14.
- Richette P., Perez-Ruiz F., Doherty M. et al. Improving cardiovascular and renal outcomes in gout: what should we target? // Nat. Rev. Rheumatol. 2014; 10. P. 654–661.
- Zhu Y., Pandya B., Choi H. Comorbidities of gout and hyperuricemia in the US general population: NHANES 2007–2008 // Am. J. Med. 2012: 125. P. 679–687.
- Ребров А. П., Магдеева Н. А. Применение амлодипина при артериальной гипертонии у больных подагрой // Саратовский научно-медицинский журнал. 2008. № 1 (19). С. 72–75.
- Ребров А. П., Магдеева Н. А. Особенности эндотелиальной дисфункции у больных подагрой и ее изменения на фоне проводимой терапии // Саратовский научно-медицинский журнал. 2008. № 3 (21). С. 59–62.
- Chang K., Yokose C., Tenner C. et al. Association between gout and aortic stenosis // Am. J. Med. 201 7; 130 (2): 230. e1–230.e8.
- Елисеев М. С., Денисов И. С., Маркелова Е. И. и др. Независимые факторы риска развития тяжелых сердечно-сосудистых осложнений у мужчин с подагрой: результаты 7-летнего проспективного исследования // Терапевтический архив. 2021. № 89 (5). С. 10–19.
- Krishnan E., Baker J. F., Furst D. E. et al. Gout and the risk of acute myocardial infarction // Arthritis Rheum. 2006 Aug; 54 (8): P. 2688–2696.
- Елисеев М. С. Обновленные рекомендации EULAR по лечению подагры. Комментарии к некоторым позициям // Научно-практическая ревматология. 2021. № 55 (6). С. 600–609.
- Елисеев М. С., Шаяхметова Р. У. Опыт применения фебуксостата у пациента с тяжелой инвалидизирующей подагрой // Современная ревматология. 2021. № 11 (3). С. 81–84.
- Елисеев М. С., Барскова В. Г., Денисов И. С. Динамика клинических проявлений подагры у мужчин (данные 7-летнего ретроспективного наблюдения) // Терапевтический архив. 2015. № 87 (5). С. 10–15.
- Елисеев М. С., Желябина О. В., Маркелова Е. И. и др. Оценка кардиоваскулярного риска при применении ингибитора интерлейкина 1 у больных тяжелой тофусной подагрой // Современная ревматология. 2016. № 10 (1). С. 7–14.
- Goicoechea M., de Vinuesa S. G., Verdalles U. et al. Effect of Allopurinol in Chronic Kidney Disease Progression and Cardiovascular Risk // Clin. J. Am. Soc. Nephrol. 2010; 5 (8): P. 1388–1393.
- Higgins P., Dawson J., Lees K. R. et al. Xanthine oxidase inhibition for the treatment of cardiovascular disease: a systematic review and meta-analysis // Cardiovasc. Ther. 2012; 30. P. 217–226.
- Dubreuil M., Zhu Y., Zhang Y. et al. Allopurinol initiation and allcause mortality in the general population // Ann. Rheum. Dis. 2015 Jul; 74 (7). P. 1368–1372.
- Xin W., Mi S., Lin Z. Allopurinol therapy improves vascular endothelial function in subjects at risk for cardiovascular diseases: a meta-analysis of randomized controlled trials // Cardiovasc. Ther. 2016; 34. P. 441–449.
- Noman A., Ang D. S., Ogston S. et al. Effect of high-dose allopurinol on exercise in patients with chronic stable angina: a randomised, placebo controlled crossover trial // Lancet. 2010; 375 (9732). P. 2161–2167.
- Givertz M. M., Anstrom K. J., Redfield M. M., Deswal A. Effects of Xanthine Oxidase inhibition in Hyperuricemic heart failure patients: the Xanthine Oxidase inhibition for Hyperuricemic heart failure patients (EXACT-HF) study // Circulation. 2015; 131. Р. 1763–1771.
- Stamp L. K., Turner R., Khalilova I. S., Zhang M. et al. Myeloperoxidase and oxidation of uric acid in gout: implications for the clinical consequences of hyperuricaemia // Rheumatology (Oxford). 2014; 53. Р. 1958–1965.
- Bredemeier M., Lopes L. M., Eisenreich M. A. et al. Xanthine oxidase inhibitors for prevention of cardiovascular events: a systematic review and meta-analysis of randomized controlled trials // BMC Cardiovasc. Disord. 2021, Feb 7; 18 (1): 24.
- Meng J., Li Y., Yuan X., Lu Y. Effects of febuxostat on insulin resistance and expression of high-sensitivity C-reactive protein in patients with primary gout // Rheumatol. Int. 2021 Feb; 37 (2). P. 299–303.
- Tsuruta Y., Kikuchi K., Tsuruta Y. et al. Febuxostat improves endothelial function in hemodialysis patients with hyperuricemia: a randomized controlled study // Hemodial. Int. 2015; 19. P. 514–520.
- Tausche A. K., Christoph M., Forkmann M. et al. As compared to allopurinol, urate-lowering therapy with febuxostat has superior effects on oxidative stress and pulse wave velocity in patients with severe chronic tophaceous gout // Rheumatol Int. 2014; 34. P. 101–119.
- Schumacher H. R. Jr., Becker M. A., Wortmann R. L. et al. Effects of febuxostat versus allopurinol and placebo in reducing serum urate in subjects with hyperuricemia and gout: a 28-week, phase III, randomized, doubleblind, parallel-group trial // Arthritis Rheum. 2008; 59 (11). P. 1540–1548.
- Becker M. A., Schumacher H. R., Espinoza L. R. et al. The urate-lowering efficacy and safety of febuxostat in the treatment of the hyperuricemia of gout: the CONFIRMS trial // Arthritis Res. 2010, 12 (2): R63.
- MacDonald T. M., Ford I., Nuki G. et al. Protocol of the Febuxostat versus Allopurinol streamlined trial (FAST): a large prospective, randomised, open, blinded endpoint study comparing the cardiovascular safety of allopurinol and febuxostat in the management of symptomatic hyperuricaemia // BMJ Open. 2014; 4: e005354.
Н. А. Магдеева, кандидат медицинских наук И. А. Романова, кандидат медицинских наук Н. М. Никитина1, доктор медицинских наук, профессор
ФГБОУ ВО СГМУ им. В. И. Разумовского МЗ РФ, Саратов
1 Контактная информация
Кардиоваскулярный риск у больных подагрой и возможные пути его снижения/ Н. А. Магдеева, И. А. Романова, Н. М. Никитина Для цитирования: Лечащий врач № 9/2018; Номера страниц в выпуске: 82-85 Теги: подагрический артрит, сердечно-сосудистые осложнения, группа риска, гипертензия
Основные симптомы и лечение подагрического артрита
Пациентов беспокоят сильнейшие боли в суставах: даже малейшие прикосновение к ним становятся непереносимым, при этом суставы сильно отекают, кожа над ними приобретает багровый оттенок и ее температура повышена. Нередко у больного повышается температура тела, появляется озноб, в анализах крови определяется повышенное содержание мочевой кислоты.
Обострение очень часто возникает внезапно, чаще ночью, и длится в среднем от двух до пяти дней, иногда проходит даже без лечения. Однако спустя некоторое время боль вновь может вернуться. Интервалы между приступами становятся короче, а сами приступы более продолжительными.
У 10% пациентов после первого приступа заболевания наступает ремиссия (она может длиться до 10 лет и более). У остальных больных могут возникать рецидивы два – три раза в год. При каждом последующем приступе количество вовлеченных в процесс суставов увеличивается, а рецидивы становятся более тяжелыми и длительными.
Наличие узелков-тофусов на кистях, стопах, а также под кожей на ушных раковинах и на задней поверхности локтевых суставов является проявлением хронической форме подагры, так как они обычно появляются не ранее трех и более лет после первой подагрической атаки и количество их может быть различно. Иногда узелки-тофусы образуются не только под кожей, но и в почках, и других внутренних органах (это обычно выявляется при УЗИ, КТ).
Очень часто подагрический артрит суставов сочетается с сахарным диабетом, ожирением и гипертонической болезнью, атеросклерозом. У 1/3 больных подагрой развивается мочекаменная болезнь, иногда развивается почечная недостаточность. Все эти заболевания взаимно отягощают друг друга. Но у некоторых больных приступ мочекаменной болезни бывает первым проявлением подагры, которая выявляется после обследования больного по поводу мочекаменной болезни.